题目内容
50g镁、锌、铁的混合物与足量的稀硫酸反应得到混合溶液,蒸发后得到218g固体(已换算成无水硫酸盐).则反应产生氢气的质量是( )
A.2g B.3g C.3.5g D.4.5g
【考点】质量守恒定律及其应用;有关化学式的计算和推断.
【专题】多步反应的关系.
【分析】已知Mg→MgSO4; Zn→ZnSO4; Fe→FeSO4.并且可知道,这个变化中,增加的质量是硫酸根的质量218g﹣50g=168g,在H2SO4中 氢元素与硫酸根的质量比为2:96.
【解答】解:设生成氢气的质量为x,根据关系式A→ASO4→SO4→H2↑,
则2:96=x:168g
x=3.5g;故选C.
【点评】运用质量守恒定律,了解物质反应前后有什么不同,从中找出规律

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
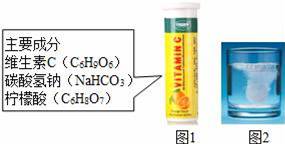
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、
N2.
小明说:不可能含有N2,因为 .
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,
H2易燃易爆,CO 有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
【得出结论】
(1)由实验①可知,该气体中肯定含有 .写出该反应的化学方程式 .
(2)由实验② (填“能”或“不能”)确定该气体中不含氧气.
探究二:维C泡腾片溶液的酸碱性.向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显 性.


 P2O5 B.4Fe+3O2
P2O5 B.4Fe+3O2