题目内容
在托盘天平的两个托盘上分别放有两个质量相同的烧杯,其中都盛有50g 19.6%的稀硫酸,天平平衡.当向两个烧杯中分别加入下列物质后,天平仍平衡的是( )
| A、Zn和Fe各1g |
| B、Zn和Fe各3g |
| C、Zn和Fe各5g |
| D、Zn和Fe各7g |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据该题目将化学反应与托盘天平平衡结合在一起.两盘中酸和金属质量相等,完全反应,天平仍平衡则产生氢气相等.由硫酸的质量求出反应的铁和锌的质量进行解答.
解答:解:设消耗50g 19.6%的稀硫酸,需要锌的质量为x,需要铁的质量为y,则有
Zn+H2SO4═ZnSO4+H2↑
65 98
x 50g×19.6%
=
x=6.5g
Fe+H2SO4═FeSO4+H2↑
56 98
y 50g×19.6%
=
y=5.6g
所以当Zn和Fe各1g、Zn和Fe各3g、Zn和Fe各5g时,硫酸都有剩余,所以生成的氢气不相等,天平不平衡;
而当Zn和Fe各7g时,金属过量,硫酸全部反应,生成氢气的质量相等,所以天平仍平衡.
故选D.
Zn+H2SO4═ZnSO4+H2↑
65 98
x 50g×19.6%
| 65 |
| x |
| 98 |
| 50g×19.6% |
x=6.5g
Fe+H2SO4═FeSO4+H2↑
56 98
y 50g×19.6%
| 56 |
| y |
| 98 |
| 50g×19.6% |
y=5.6g
所以当Zn和Fe各1g、Zn和Fe各3g、Zn和Fe各5g时,硫酸都有剩余,所以生成的氢气不相等,天平不平衡;
而当Zn和Fe各7g时,金属过量,硫酸全部反应,生成氢气的质量相等,所以天平仍平衡.
故选D.
点评:金属与酸反应后天平平衡的问题是中考常考查的题目,完成此类题目,要分清题干提供的信息,确定是根据酸还是金属的质量进行求算.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
将质量分数为30%和10%的KNO3溶液混合,配制成质量分数为20%的KNO3溶液,应取这两种溶液的质量比为( )
| A、1:3 | B、2:3 |
| C、1:1 | D、3:1 |
下列有关物质燃烧现象的描述,正确的是( )
| A、氢气在空气中燃烧产生大量白烟 |
| B、镁条在空气中燃烧发出耀眼的白光 |
| C、铁丝在氧气中燃烧发出明亮的火焰 |
| D、木炭在氧气中燃烧发出白光,生成二氧化碳 |
如图为某化工企业生产流程示意图,下列说法正确的是( ) 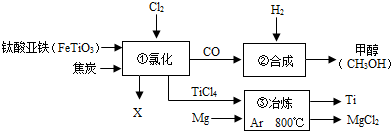

| A、钛酸亚铁(FeTiO3)中钛元素为+3 | ||||
B、①中反应为:2FeTiO3+6C+7Cl2
| ||||
| C、③中氩气(Ar)作保护气,反应类型为置换反应 | ||||
| D、②中为使原料全部转化为甲醇,理论上CO和H2投料的质量比为1:2 |
对实验室制取氧气的实验,请你判断,下列说法错误的是( )
| A、可用加热高锰酸钾来制取氧气 |
| B、用酒精灯的内焰加热试管 |
| C、用排水法收集氧气 |
| D、实验后的试管,要洗涤干净存放 |
如果1g水中含有m个氢原子,则阿伏加德罗常数是( )
A、
| ||
| B、9m | ||
| C、2m | ||
| D、18m |
下列曲线与实验事实相一致的是( )
A、 向一定体积HCl溶液中滴加NaOH溶液 |
B、 t°C向一定量饱和NaCl溶液中不断加入蔗糖 |
C、 向一定量的HCl和CaCl2混合液中不断加入Na2CO3溶液 |
D、 向CuCl2和H2SO4的混合液中加入过量Ba(OH)2溶液 |
下列物质属于纯净物的是( )
| A、干净的空气 | B、食盐水 |
| C、液氧 | D、人体呼出的气体 |