题目内容
石灰石15g(含杂质,杂质不跟稀盐酸反应)与100g稀盐酸酸在烧杯中完全反应,反应后称得烧杯中物质总质量为110.6g.
(1)石灰石中碳酸钙的质量为 ;
(2)求所用盐酸的质量分数.
(1)石灰石中碳酸钙的质量为
(2)求所用盐酸的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据质量守恒定律,反应前后物质的总质量相等,可由反应前后质量差计算出反应放出二氧化碳气体的质量;然后再利用化学方程式计算石灰石中碳酸钙质量.
(2)根据二氧化碳气体的质量;再利用化学方程式计算所用盐酸中溶质的质量即可解答.
(2)根据二氧化碳气体的质量;再利用化学方程式计算所用盐酸中溶质的质量即可解答.
解答:解:(1)生成二氧化碳的质量=100g+15g-110.6g=4.4g
设15g石灰石中碳酸钙的质量为x,所用盐酸中溶质的质量为y;
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 4.4g
=
,
=
解之得 x=10g,y=7.3g
(2)所用盐酸的质量分数为:
×100%=7.3%.
答:(1)石灰石中所含碳酸钙的质量为10g.
(2)所用盐酸的质量分数为7.3%.
设15g石灰石中碳酸钙的质量为x,所用盐酸中溶质的质量为y;
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 73 44
x y 4.4g
| 100 |
| x |
| 44 |
| 4.4g |
| 73 |
| y |
| 44 |
| 4.4g |
解之得 x=10g,y=7.3g
(2)所用盐酸的质量分数为:
| 7.3g |
| 100g |
答:(1)石灰石中所含碳酸钙的质量为10g.
(2)所用盐酸的质量分数为7.3%.
点评:在任何与周围隔绝的体系中,不论发生何种变化或过程,其总质量始终保持不变.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
下列有关水的知识中,错误的是( )
| A、用过滤的方法可使浑浊的河水净化为纯净水 |
| B、硬水中含较多的可溶性钙、镁化合物,软水中则不含或少含 |
| C、用煮沸或蒸馏的方法能降低水的硬度 |
| D、用加肥皂水的方法可鉴别硬水和软水 |
下列各组物质对应的鉴别方法正确的是( )
| A、硬水和软水--观察是否澄清 |
| B、黄金和假黄金(铜锌合金)--滴加硫酸铜溶液 |
| C、合成纤维和羊毛--用手触摸 |
| D、聚乙烯塑料和聚氯乙烯塑料--观察颜色 |
碳元素与氧元素的本质区别是( )
| A、电子数不同 |
| B、质子数不同 |
| C、中子数不同 |
| D、最外层电子数不同 |
用分子的观点对下列现象的解释,不正确的是( )
| A、六月槐花飘香──分子在不断地运动 |
| B、50ml水和50ml酒精混合体积小于100ml──分子间有间隔 |
| C、食物腐烂──分子本身发生了变化,变成别的物质的分子 |
| D、变瘪的乒乓球放在热水中又鼓起来──分子的大小随温度变化而改变 |
下列变化只发生物理变化的是( )
| A、金属生锈 | B、石蜡熔化 |
| C、纸张燃烧 | D、二氧化碳溶于水 |
自来水的净化主要包括以下过程,其中发生化学变化的是( )
| A、自然沉淀 | B、砂层过滤 |
| C、活性炭吸附 | D、杀菌消毒 |
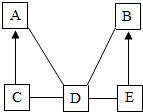 A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质;C是红棕色固体;E是水溶液可使酚酞试液变为红色的盐.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题:
A、B、C、D、E是初中化学中常见的不同类别的物质(物质按单质、氧化物、酸、碱、盐分类).已知A是单质;C是红棕色固体;E是水溶液可使酚酞试液变为红色的盐.图中“-”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质(部分反应物、生成物及反应条件已略去).回答下列问题: