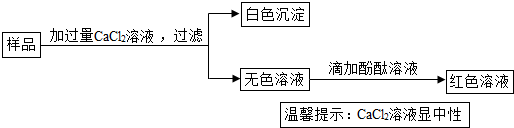
题目内容
17. 某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);步骤Ⅰ:连接实验装置并检查装置气密性.
步骤Ⅱ:向b中加入质量为mg的石灰石样品粉末,由注射器a向b中缓缓加入足量的稀盐酸,至b中不再有气体产生时,夹紧弹簧夹,立即移除d中导管,准确读数取并记录量筒内水的体积.
步骤Ⅲ:将b中剩余固体经过滤等操作,准确称量并记录b中剩余固体的质量为ng.
步骤IV:该小组的甲同学根据反应前后b中固体物质的质量,计算样品中碳酸钙的质量分数;乙同学认定量筒内测得水的体积即为反应生成气体的体积,并利用该气体在常温下的密度,根据化学方程式进行相关计算,得到样品中碳酸钙的质量分数.
请回答下列问题:
(1)b中发生反应的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)步骤Ⅲ中,正确的操作顺序是:过滤、洗涤、干燥、称量、写出据此计算石灰石样品中碳酸钙的质量分数表达式$\frac{m-n}{m}$×100% (用题中所给字母表示).
(3)通过误差分析,兴趣小组发现乙同学所用数据不可靠.造成该数据不可靠的原因及其对计算结果的影响是:
①步骤Ⅱ中移出d中的导管内留存有水,导致计算结果偏小.
②二氧化碳有少量的溶解,导致计算结果偏小.
【继续分析】你若还有关于乙同学所用数据不可靠的原因及其对计算结果的影响,请继续写在下面
③步骤Ⅱ中,反应可能放热,导致计算结果偏大.
④注入的稀盐酸占有一定体积,导致计算结果偏大.
分析 (1)根据石灰石(主要成分碳酸钙)与稀盐酸反应生成氯化钙、水和二氧化碳进行分析;
(2)根据固液分离的操作以及物质含量的计算考虑;
(3)根据实验过程中可能出现的错误操作考虑.
解答 解:(1)石灰石(主要成分碳酸钙)与稀盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.
(2)从杂质和氯化钙溶液的混合物中得到杂质,先进行过滤,得到带有氯化钙溶液的杂质,再进行洗涤除去表面的氯化钙溶液,再进行干燥除去水即可;
石灰石样品中碳酸钙的质量为mg-ng,石灰石样品中碳酸钙的质量分数为$\frac{m-n}{m}$×100%;
(3)①步骤Ⅱ中移出d中的导管内留存有水,则导致量筒中水的体积小于二氧化碳的体积,使计算得碳酸钙质量减小,导致计算结果偏小;
②由于二氧化碳能溶于水,二氧化碳有少量的溶解,造成测得二氧化碳的体积,使计算得碳酸钙质量减小,导致计算结果偏小;
【继续分析】
由于碳酸钙与盐酸反应生成氯化钙、水和氢气时,放出热量,如果没等冷却到室温,根据热涨冷缩的原理可知进入量筒中水偏多,所以误认为得到的二氧化碳多,计算的结果就偏大;
注入的稀盐酸的体积会多排出一部分气体,误认为得到的二氧化碳多,计算的结果就偏大.
故答案为:(1)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(2)干燥,$\frac{m-n}{m}$×100%;
(3)①小;
②二氧化碳有少量的溶解,小;
③步骤Ⅱ中,反应可能放热,大;
④注入的稀盐酸占有一定体积,大.
点评 本题容易出错的地方是对实验结果的评价,要知道锌与硫酸反应放出热量,会造成相应的误差,必须冷却到室温才能进行观察和计算.

练习册系列答案
相关题目
8.从分子的角度分析,对下列现象解释错误的是( )
| A. | “墙内开花,墙外香”--分子在不断地运动 | |
| B. | 湿衣服晾在有太阳的地方比晾在没有太阳的地方容易干--温度高分子的运动速度加快 | |
| C. | 热胀冷缩--分子的大小随着温度的改变而改变 | |
| D. | 水电解生成氢气和氧气--在化学变化中,分子分解成原子,原子又构成新的分子 |
7. 元素周期表是学习科学的重要工具.如图是元素周期表中的一格,对图中信息的理解错误的( )
元素周期表是学习科学的重要工具.如图是元素周期表中的一格,对图中信息的理解错误的( )
 元素周期表是学习科学的重要工具.如图是元素周期表中的一格,对图中信息的理解错误的( )
元素周期表是学习科学的重要工具.如图是元素周期表中的一格,对图中信息的理解错误的( )| A. | “7”为原子序数 | B. | “N”为元素符号 | ||
| C. | “氮”为元素名称 | D. | “14.01”为原子质量 |
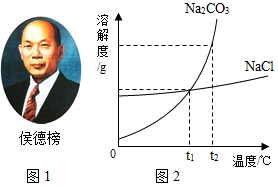 1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,该方法是以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应:
1926年,我国著名化学家侯德邦先生创立了侯氏制碱法,促进了世界制碱技术的发展,该方法是以从海水中提取出来的食盐为主要原料制取纯碱.其生产过程中有下列反应: 某元素原子的结构示意图如图,该元素原子核内有11 个质子,它属于金属元素,在化学反应中易失去电子形成阳离子(填阴或阳),该元素原子形成的离子符号为Na+,它与硫元素形成的化合物的化学式为Na2S.
某元素原子的结构示意图如图,该元素原子核内有11 个质子,它属于金属元素,在化学反应中易失去电子形成阳离子(填阴或阳),该元素原子形成的离子符号为Na+,它与硫元素形成的化合物的化学式为Na2S.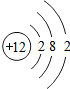 用化学用语填空:
用化学用语填空: