题目内容
19. 为测定某铁粉样品(含少量木炭粉)中铁的含量,往盛有219g稀盐酸的烧杯中不断加入铁粉样品,测得生成氢气的质量与所加铁粉样品的质量关系如图所示.
为测定某铁粉样品(含少量木炭粉)中铁的含量,往盛有219g稀盐酸的烧杯中不断加入铁粉样品,测得生成氢气的质量与所加铁粉样品的质量关系如图所示.(1)稀盐酸恰好完全反应时,生成氢气的质量为0.6g.
(2)求219g稀盐酸中溶质的质量分数.
分析 (1)从图象可直接读出最终生成氢气的质量;
(2)依据稀盐酸恰好完全反应时,生成氢气的质量求出稀盐酸中溶质的质量,再根据溶质质量分数计算公式计算即可.
解答 解:(1)由图象可知最终生成氢气的质量是0.6g;
(2)设盐酸溶液中溶质的质量为x
Fe+2HCl=FeCl2+H2↑
73 2
x 0.6g
$\frac{73}{2}=\frac{x}{0.6g}$解得:x=21.9g
219g稀盐酸中溶质的质量分数=$\frac{21.9g}{219g}×100%$=10%
答:(1)0.6;(2)稀盐酸溶液中溶质的质量分数为10%.
点评 解答此类问题的根本点在于对反应图象的曲线进行分析,曲线的折点表示此时恰好完全反应.

练习册系列答案
相关题目
7.下列知识整理的内容有错误的一组是( )
| A、除杂的方法 | B、化学与健康 |
| ①粗盐提纯--溶解、过滤、蒸发 ②木炭粉中混有铁粉--用磁铁吸引 ③CO2中混有CO--通过灼热的氧化铜 | ①人体缺铁会引起贫血症 ②多吃水果蔬菜利于补充维生素 ③用活性炭净水器可净化饮用水 |
| C、实验记录 | D、化学物质与俗名 |
| ①用10mL量筒量取7.25mL水 ②用pH试纸测得苹果汁的pH为3.2 ③用托盘天平称取5.6g铁粉 | ①固体二氧化碳-干冰 ②干燥剂氧化钙-生石灰 ③氢氧化钠-烧碱、火碱、苛性钠 |
| A. | A | B. | B | C. | C | D. | D |
14.下列叙述正确的是( )
| A. | 催化剂是能改变化学反应速率而本身的质量和性质都不变的物质 | |
| B. | 氢、碳、氧的原子核都由质子和中子构成 | |
| C. | pH=0的溶液呈中性 | |
| D. | 饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液 |
4.下列食品中,富含糖类的是( )
| A. | 鸡蛋 | B. | 黄瓜 | C. | 豆油 | D. | 土豆 |
9.下列图象能正确反映其对应操作的是( )
| A. | 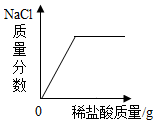 一定量的NaOH溶液中逐滴加入稀盐酸 | |
| B. | 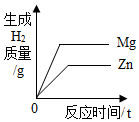 等质量、等质量分数的稀硫酸中分别加入足量的镁粉和锌粉 | |
| C. | 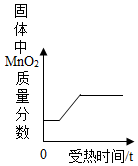 用适量KClO3和MnO2的混合物加热制取O2 | |
| D. | 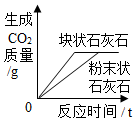 等质量、不同形状的石灰石中分別加入足量相同的稀盐酸 |
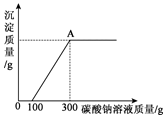 为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液224.4克于烧杯中,在不断振荡的条件下,向其中逐滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示.经测定A中只含有一种溶质.根据题中有关信息和图象分析回答下列问题.
为了探究石灰石与稀盐酸反应制备二氧化碳后的废液中的溶质成分,将废液过滤,取滤液224.4克于烧杯中,在不断振荡的条件下,向其中逐滴加质量分数为10.6%的碳酸钠溶液直至过量,有关的变化如图所示.经测定A中只含有一种溶质.根据题中有关信息和图象分析回答下列问题. )和118号(Og
)和118号(Og )为化学新元素.其中,“115号(Mc 镆)”中115表示原子的原子序数,Mc表示的微观意义是一个镆原子.
)为化学新元素.其中,“115号(Mc 镆)”中115表示原子的原子序数,Mc表示的微观意义是一个镆原子.