题目内容
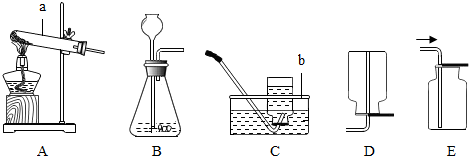
17.下列图示的基本操作正确的是( )| A. |  验满二氧化碳 | B. |  倾倒液体 | C. |  称量固体 | D. | 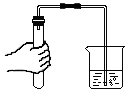 检查装置气密性 |
分析 A、根据二氧化碳验满的方法进行分析判断;
B、根据液体药品的取用方法进行分析判断;
C、根据托盘天平的使用方法进行分析判断;
D、根据检查装置气密性的方法进行分析判断.
解答 解:A、检验二氧化碳是否集满时,应将燃着的木条放在集气瓶口,而不是倒入澄清的石灰水,图中所示操作错误;
B、取用液体药品时,瓶塞要倒放,标签要对准手心,瓶口紧挨,图中所示操作错误;
C、使用托盘天平称物时:左托盘放称量物,右托盘放砝码,图中所示操作错误;
D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气,图中所示操作正确.
故选:D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
相关题目
15.2013上海21所学校采购的毒校服,使用了含有毒化学品联苯胺的染料和助剂,其中苯胺(化学式为C6H7N).下列有关说法正确的是( )
| A. | 苯胺是有机化合物 | B. | 苯胺分子中共有14个原子 | ||
| C. | 苯胺中C,N两种元素的质量比为6:1 | D. | 苯胺中氢原子的质量分数最大 |
5.溶液在生命活动和生产、生活中都起到十分重要的作用.
(1)将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶质为I2,溶剂为C2H5OH.(写出物质化学式)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
实验a、b、c、d中,有未被溶解的KNO3固体析出的实验是d(填写实验编号).
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,应加入水的质量为150g.
(4)在硝酸亚铁和硝酸银的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,有气泡产生,则滤出的固体可能有镁粉(填名称),滤液中可能含有的溶质Fe(NO3)2(填化学式).
(1)将少量下面的调味品加入水中,不能形成溶液的是D.
A.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶质为I2,溶剂为C2H5OH.(写出物质化学式)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 | a | b | c | d |
| 加入KNO3固体的质量 | 45 | 50 | 55 | 60 |
| 所得溶液的质量 | 95 | 100 | 105 | 105 |
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c=d.
④取实验b所得溶液,若使其质量分数变为20%,在不改变温度的情况下,应加入水的质量为150g.
(4)在硝酸亚铁和硝酸银的混合溶液中加入一定量的镁粉,充分反应后过滤,向滤出的固体中滴加稀盐酸,有气泡产生,则滤出的固体可能有镁粉(填名称),滤液中可能含有的溶质Fe(NO3)2(填化学式).
2.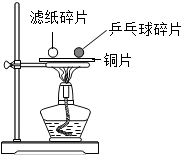 如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
 如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )
如图,把同样大小的滤纸碎片和乒乓球碎片放在薄铜片的两侧,加热,下列实验现象或结论错误的是( )| A. | 实验说明燃烧的条件之一是温度达到可燃物的着火点 | |
| B. | 铜片受热后变黑,可能是因为产生了氧化铜 | |
| C. | 实验过程中滤纸碎片先燃烧,乒乓球碎片后燃烧 | |
| D. | 实验说明铜有导热性 |
6.下列说法正确的是( )
| A. | 根据质量守恒定律,1 L氢气和1 L氧气反应能生成2 L水 | |
| B. | 蜡烛完全燃烧后,蜡烛没有了,不违背质量守恒定律 | |
| C. | 只有固体、液体间反应遵守质量守恒定律 | |
| D. | 铁在氧气中燃烧,生成四氧化三铁质量等于参加反应的铁丝的质量 |
7.某粒子的结构示意图为 ,则下列有关该粒子的判断中,错误的是( )
,则下列有关该粒子的判断中,错误的是( )
 ,则下列有关该粒子的判断中,错误的是( )
,则下列有关该粒子的判断中,错误的是( )| A. | 有 2 个电子层,x 的值一定为 10 | |
| B. | 可能是原子、阴离子或阳离子 | |
| C. | 化合价可能是负价、0 或正价 | |
| D. | 核内质子数和核外电子数之差可能是正数、0 或负数 |