题目内容
15.某兴趣小组围绕“实验室制取氧气”进行了一系列探究活动:(1)药品选择:下列物质中不能作为实验室制取氧气反应物的是C(填字母).
A.水 B.过氧化氢 C.氯化钾 D.高锰酸钾(KMnO4)
原因是氯化钾中无氧元素.
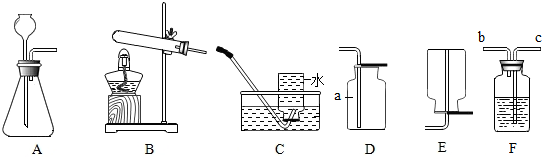
(2)装置连接,所需的一些实验装置如图1所示:
仪器a的名称是分液漏斗;选择气体收集方法时,气体的下列性质:A.颜色 B.可燃性 C.溶解性 D.密度,必须考虑的是CD(填字母);要制取并收集一瓶干燥的氧气,所选装置的连接顺序为ADB(填装置字母序号).
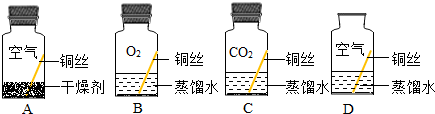
(3)气体检验:如图2甲装置中带火星的木条很难复燃,乙装置中带火星的木条较易复燃,原因是乙装置中将生成的氧气通过浓硫酸干燥,除去了其中的水蒸气等.
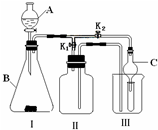
(4)实验探究:如图3所示,向三支试管中分别滴加浓度相同的三种溶液,观察可见:实验①中无明显现象,实验②中产生气泡,实验③中产生气泡更快,据悉你能得出的结论是硫酸铜和氧化铁能加快过氧化氢的分解.

分析 (1)根据质量守恒定律,制取氧气,反应物中必须有氧元素解答;根据实验室中制取氧气的原理、干燥收集方法以及氧气的验满方法来分析;
(2)根据实验室常用仪器解答;根据气体的密度和溶解性选择收集装置;根据实验室中制取氧气的原理、干燥收集方法以及氧气的验满方法来分析;
(3)根据乙装置中将生成的氧气通过浓硫酸干燥,除去了其中的水蒸气等解答;
(4)根据促进反应加快的因素解答.
解答 解:(1)据质量守恒定律,制取氧气,反应物中必须有氧元素,氯化钾中无氧元素,故选C;
(2)根据实验室常用仪器可知:仪器a的名称是分液漏斗;选择气体收集方法时,必须考虑的是密度和溶解性;过氧化氢在二氧化锰的催化作用下分解为水和氧气;因为反应物是固体与液体,在常温下进行,选择装置A来制取,收集一瓶干燥的氧气,用浓硫酸来进行干燥,用向上排空气法来收集;
(3)如图2甲装置中带火星的木条很难复燃,乙装置中带火星的木条较易复燃,原因是:乙装置中将生成的氧气通过浓硫酸干燥,除去了其中的水蒸气等
(4)如图3所示,向三支试管中分别滴加浓度相同的三种溶液,观察可见:实验①中无明显现象,实验②中产生气泡,实验③中产生气泡更快,据悉你能得出的结论是硫酸铜和氯化铁能加快过氧化氢的分解.
答案:
(1)C;氯化钾中无氧元素;
(2)分液漏斗;CD;ADB;
(3)乙装置中将生成的氧气通过浓硫酸干燥,除去了其中的水蒸气等;
(4)硫酸铜和氯化铁能加快过氧化氢的分解.
点评 本题考查了装置的选择、化学方程式的书写、实验装置的改进,难度不大.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.环境保护是2016年两会热点话题,下列说法错误的是( )
| A. | 使用无磷洗衣粉预防水体富营养化 | |
| B. | 淘汰黄标车减少汽车尾气污染 | |
| C. | 深埋废旧电池减少重金属污染 | |
| D. | 使用低毒、低残留农药减轻环境污染 |
7.茶叶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法错误的是( )
| A. | 单宁酸由C、H、O三种元素组成 | |
| B. | 单宁酸中氢元素质量分数最小 | |
| C. | 单宁酸中氢、氧元素的质量比为26:23 | |
| D. | 单宁酸是有机化合物 |