题目内容
13.某班同学在实验室做制取二氧化碳的实验,老师观察到了四个同学的如下操作正确的是( )| A. | 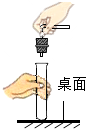 连接仪器 | B. | 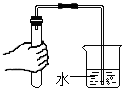 检查气密性 | C. |  取用石灰石 | D. | 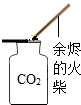 验满 |
分析 A、根据把试管放入桌面,用手拿橡皮塞硬往试管口按,易使试管压破解答;
B、根据检查气密性的方法解答;
C、根据往试管内加固体药品时,先使试管横放,将药品送入试管底部解答;
D、根据二氧化碳气体验满的方法解答.
解答 解:A、把试管放入桌面,用手拿橡皮塞硬往试管口按,易使试管压破,应左手拿试管,离开桌面,右手拿橡皮塞稍稍用力转动塞入;故错误;
B、检查气密性的方法是先把导气管放入水中,用手捂住试管一会,如果导气管口有气泡冒出,则证明气密性好,故正确;
C、往试管内加固体药品时,先使试管横放,将药品送入试管底部,图示会造成试管破裂,故错误;
D、二氧化碳气体验满的方法是用燃着的木条放在集气瓶口,如果熄灭,则证明已满,故错误.
答案:B
点评 本题考查了常见的实验操作的方法和注意事项,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
18.下列实验操作中,不正确的是( )
| A. | 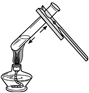 | B. | 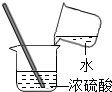 | C. | 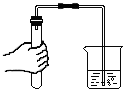 | D. |  |
2.下列属于人体必需微量元素的是( )
| A. | H | B. | Mg | C. | Ca | D. | Zn |
3.下列实验现象描述错误的是( )
| A. | 硫粉在氧气中燃烧产生的淡蓝色火焰 | |
| B. | 将带火星的木条伸入到盛有氧气的集气瓶中,木条复燃 | |
| C. | 熟石灰与(NH4)2SO4,产生有刺激性气味的气体 | |
| D. | 铝丝插入硫酸铜溶液中,铝丝表面有红色物质析出 |
 已知A、B、C、D、E为初中化学中常见的五种不同类型的物质,其中A为年产量最高的金属单质,各种物质间的反应和转化关系如图所示(“-”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质:反应条件、部分反应物和生成物已略去).请写出:
已知A、B、C、D、E为初中化学中常见的五种不同类型的物质,其中A为年产量最高的金属单质,各种物质间的反应和转化关系如图所示(“-”表示相连的两种物质之间可以发生反应,“→”表示一种物质可以转化为另一种物质:反应条件、部分反应物和生成物已略去).请写出: