题目内容
1.过氧化氢不稳定会自然分解,久置的过氧化氢溶液,其溶质的质量分数会变小.某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质的质量分数,进行实验.测得相关数据如图所示:
(1)根据质量守恒定律,反应生成氧气的质量为0.8g.
(2)二氧化锰在反应过程中起催化作用.
(3)计算该过氧化氢溶液中溶质的质量分数.(写出计算过程)
分析 过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应前后的质量差即为反应生成氧气的质量,根据氧气的质量可以计算过氧化氢的质量,进一步可以计算该过氧化氢溶液中溶质的质量分数.
解答 解:(1)根据质量守恒定律,反应生成氧气的质量为:34.0g+0.5g-33.7g=0.8g,
故填:0.8g.
(2)二氧化锰在反应过程中起催化作用.
故填:催化.
(3)设过氧化氢质量为x,
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,
68 32
x 0.8g
$\frac{68}{x}$=$\frac{32}{0.8g}$,
x=1.7g,
该过氧化氢溶液中溶质的质量分数为:$\frac{1.7g}{34.0g}$×100%=5%,
答:该过氧化氢溶液中溶质的质量分数为5%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
相关题目
16.房屋在新装修后,室内空气通常含有较多甲醛,住户要注意通风,以防中毒.下列关于甲醛(HCHO)的说法,正确的是( )
| A. | 甲醛是一种酸 | |
| B. | 甲醛是由氢元素、氧元素和碳元素组成的一种氧化物 | |
| C. | 甲醛有挥发性 | |
| D. | 甲醛分子中碳、氢、氧各原子的个数比为1:1:2 |
6.如图所示装置的集气瓶被誉为“万能瓶”.下列说法错误的是( )
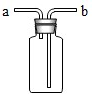

| A. | 收集氢气时应从b口进入,瓶内空气从a口排出 | |
| B. | 收集二氧化碳时应从a口进入,瓶内空气从b口排出 | |
| C. | 当被收集的气体从a口进入时,瓶内空气从b口排出,相当于向上排出空气法收集气体 | |
| D. | 当被收集的气体从b口进入时,瓶内空气从a口排出,相当于向上排出空气法收集气体 |
10.下列变化属于化学变化的是( )
| A. | 石蜡熔化 | B. | 酒精挥发 | C. | 粮食酿酒 | D. | 干冰升华 |