题目内容
13.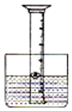 某化学兴趣小组,设计了如右图所示装置来研究空气中氧气的体积分数:用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升.向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.
某化学兴趣小组,设计了如右图所示装置来研究空气中氧气的体积分数:用一个50mL量筒倒扣在水中,使量筒内外液面均位于40mL处.量筒内浮着一个铜制的小船,船中放有足量白磷.现把浓硫酸缓缓倒入水中并搅拌.一会儿,白磷发生自燃,量筒内液面上升.向水槽内加水直至量筒内外液面相平,读出此时液面所对刻度.(1)加入浓硫酸的目的是浓硫酸溶于水放热,使温度达到白磷的着火点以上;
(2)放白磷的小船用铜做的原因是铜导热性好且化学性质稳定;
(3)最终,液面大约位于量筒刻度32mL处;
(4)该兴趣小组选用的仪器有何缺陷?量筒不能用作反应容器.
分析 (1)浓硫酸溶于水放热,为反应提供热量;
(2)根据金属铜具有良好的导热性,并且化学性质稳定来回答此题;
(3)从实验的目的出发来回答就容易了,此实验目的是研究空气中所含氧气的体积;
(4)量筒是用来测量液体的体积的,不能用作反应容器.
解答 解:(1)浓硫酸溶于水时发出大量的热,使得温度升高,温度达到白磷的着火点以上,白磷就会燃烧,从而达到实验的目的,故答案为:浓硫酸溶于水放热,使温度达到白磷的着火点以上;
(2)金属铜具有良好的导热性,并且化学性质稳定,不会影响实验的准确性,故答案为:铜导热性好且化学性质稳定;
(3)此实验是为了研究空气中所含氧气的体积,根据教材所学氧气约占空气总体积的五分之一这一结论,可以计算40mL-40mL×$\frac{1}{5}$=32mL; 故答案为:32mL;
(4)根据教材所学我们知道,量筒是用来测量液体的体积的,不能用作反应容器,故答案为:量筒不能用作反应容器.
故答案为:
(1)浓硫酸溶于水放热,使温度达到白磷的着火点以上;
(2)铜导热性好且化学性质稳定;
(3)32;
(4)量筒不能用作反应容器.
点评 此题是一道综合实验题,所考查的知识点较多,而且十分细致,需要同学们对实验十分熟悉才可以准确回答.

练习册系列答案
相关题目
3.对下列物质的俗称,理解错误的是( )
| A. | 干冰不是冰 | B. | 纯碱不是碱 | C. | 水银不是银 | D. | 醋酸不是酸 |
1.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如表所示).他从瓶中倒出50毫升用于配制成稀硫酸,问:
(1)这50毫升浓硫酸的质量为92克,其中含溶质硫酸90.16克.
(2)他将这50毫升浓硫酸与200克水均匀混合,求所得稀硫酸的质量分数.(结果保留一位小数)
(3)若实验室要配制630g溶质质量分数28%的稀硫酸,则需要这瓶溶质质量分数为98%的浓硫酸毫升?
| 浓硫酸(H2SO4) 500毫升 | |
| 浓度(质量分数) | 98% |
| 密度 | 1.84克•厘米-3 |
| 相对分子质量 | 98 |
| 强腐蚀性,阴冷,密封贮藏 | |
(2)他将这50毫升浓硫酸与200克水均匀混合,求所得稀硫酸的质量分数.(结果保留一位小数)
(3)若实验室要配制630g溶质质量分数28%的稀硫酸,则需要这瓶溶质质量分数为98%的浓硫酸毫升?
18.酸、碱、盐3类物质,它们的共同点是( )
①都能溶于水
②都含有氧元素
③都含有金属离子
④都是化合物.
①都能溶于水
②都含有氧元素
③都含有金属离子
④都是化合物.
| A. | ①②④ | B. | ②④ | C. | ②③④ | D. | ④ |
2.将一定质量金属X的粉末放入盛有Fe(NO3)2溶液的烧杯中,充分反应后溶液呈无色;继续向烧杯中加入一定量的AgNO3溶液,待充分反应后过滤,得浅绿色滤液和滤渣.根据实验分析,以下结论正确的是( )
| A. | 金属活动性顺序:Fe>X>Ag | |
| B. | 滤渣中一定含有Fe | |
| C. | 滤液中一定含有X的阳离子和Fe2+ | |
| D. | 向滤液中滴加稀盐酸,一定产生白色沉淀 |
3.下列各组离子,在同一溶液中能大量共存的是( )
| A. | H+、Cl-、HCO${\;}_{3}^{-}$ | B. | Na+、Ca2+、OH- | ||
| C. | Ba2+、Cl-、CO${\;}_{3}^{2-}$ | D. | H+、Mg2+、SO${\;}_{4}^{2-}$ |