题目内容
 科学探究:铁、铜、银是初中化学课上学过的三种金属,实验设计如图所示.请回答:
科学探究:铁、铜、银是初中化学课上学过的三种金属,实验设计如图所示.请回答:(1)猜想该实验在探究的问题是
(2)所用的科学探究的方法是
(3)观察到的实验现象是
考点:金属的化学性质
专题:金属与金属材料
分析:金属和盐溶液发生置换反应必须具备:在金属活动性顺序中,只有前面的金属可以把排在它后面的金属从盐溶液中置换出来,钾、钙、钠除外;根据金属活动性顺序可以设计实验来验证金属的活动性强弱
解答:解:从图中不难看出,把铁丝和银丝都放到了硫酸铜溶液中,是为了探究三种金属的活动性强弱的;由于铁的活动性比铜强,因此在铁丝表面会有红色物质生成,即铁可以把铜从盐溶液中置换出来,从而证明铁的活动性比铜强,同理证明银的活动性比铜弱,故答案为:(1)探究铁、铜、银的金属活动性强弱;(2)比较法、实验探究法;(3)铁丝表面覆盖一层红色物质,银丝表面无变化;三种物质的金属活动性:铁>铜>银.
点评:本题主要考查了金属活动性顺序的探究,有关反应的实验现象等方面的内容.

练习册系列答案
相关题目
将3.25g锌片和等质量的铁片分别与足量的盐酸反应,反应结束后,均收集到0.1g氢气,则可推断( )
| A、锌片和铁片均属于纯净物,不含杂质 |
| B、锌片和铁片均可能含有杂质 |
| C、锌片不含杂质,铁片可能含有杂质锌 |
| D、锌片不含杂质,铁片可能含有杂质铜 |
根据如图三种微粒结构示意图,所获取信息不正确的是( )


| A、①表示的是原子,②表示的是离子 |
| B、它们表示两种元素 |
| C、②③化学性质相同 |
| D、①②形成的化合物为AlN |
将下列两种物质放在烧杯里混合,混合前后烧杯里的物质质量不变的是( )
①稀盐酸和烧碱溶液 ②Na2CO3溶液和稀HNO3
③碳酸钙固体和稀盐酸 ④NaOH溶液和硫酸铜溶液.
①稀盐酸和烧碱溶液 ②Na2CO3溶液和稀HNO3
③碳酸钙固体和稀盐酸 ④NaOH溶液和硫酸铜溶液.
| A、只有① | B、只有④ |
| C、只有②③ | D、只有①④ |
汽油的质量取决于异辛烷含量,辛烷值越高,汽油的抗爆性越好.已知异辛烷燃烧的化学方程式:2异辛烷+25O2
16CO2+18H2O,则异辛烷的化学式为( )
| ||
| A、C16H36 |
| B、C8H16 |
| C、C8H18 |
| D、C2H5OH |
如图所示微观变化的化学反应类型,与下列反应的反应类型一致的是( ) 

| A、化合反应 | B、分解反应 |
| C、置换反应 | D、复分解反应 |
下列实验操作错误的是( )
A、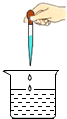 用滴管滴加试剂 |
B、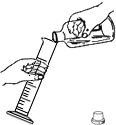 液体的量取 |
C、 检验氢气的纯度 |
D、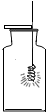 铁丝在氧气中燃烧 |