题目内容
14.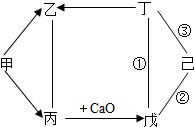 甲、乙、丙、丁、戊、己是初中化学中常见的一些物质,它们之间存在如图所示的相互关系(“-”表示在一定条件下能相互反应,“→”表示在一定条件下能发生转化),己知乙是一种气体,能使澄清的石灰水变浑浊;甲、乙、丙三种物质含有一种相同的元素,且甲是一种单质;乙和丁不含相同的元素,反应①、②、③中,一个有白色沉淀产生,一个有气体放出,一个无明显现象.
甲、乙、丙、丁、戊、己是初中化学中常见的一些物质,它们之间存在如图所示的相互关系(“-”表示在一定条件下能相互反应,“→”表示在一定条件下能发生转化),己知乙是一种气体,能使澄清的石灰水变浑浊;甲、乙、丙三种物质含有一种相同的元素,且甲是一种单质;乙和丁不含相同的元素,反应①、②、③中,一个有白色沉淀产生,一个有气体放出,一个无明显现象.(1)写出甲物质的一种用途支持燃烧.
(2)己物质所属的类别为盐(填“酸”“碱”“盐'”或“氧化物”).
(3)写出丁→乙的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑.
分析 根据题干提供的信息进行分析解答,乙是一种气体,能使澄清的石灰水变浑浊,故乙是二氧化碳;甲、乙、丙三种物质含有一种相同的元素,且甲是一种单质,能转化生成乙和丙,丙能与氧化钙反应,故丙是水,生成的戊是氢氧化钙,故甲是氧气;氢氧化钙能与丁和已反应,且丁能转化生成二氧化碳,乙和丁不含相同的元素,故丁可能是盐酸氢氧化钙与盐酸的反应没有现象;戊能与盐酸和氢氧化钙反应,且反应一个有白色沉淀产生,一个有气体放出,故已是碳酸钠,据此解答.
解答 解:乙是一种气体,能使澄清的石灰水变浑浊,故乙是二氧化碳;甲、乙、丙三种物质含有一种相同的元素,且甲是一种单质,能转化生成乙和丙,丙能与氧化钙反应,故丙是水,生成的戊是氢氧化钙,故甲是氧气;氢氧化钙能与丁和已反应,且丁能转化生成二氧化碳,乙和丁不含相同的元素,故丁可能是盐酸氢氧化钙与盐酸的反应没有现象;戊能与盐酸和氢氧化钙反应,且反应一个有白色沉淀产生,一个有气体放出,故已是碳酸钠,带入框图,推断合理;
(1)甲是氧气,能支持燃烧,故填:支持燃烧;
(2)己物质是碳酸钠,属于盐类物质,故填:盐;
(3)盐酸能与碳酸钙反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑.
点评 本题为框图式物质推断题,解答本题的关键是掌握物质的性质以及物质间反应的实验现象,找准解题的突破口,可以快速的完成推断.

练习册系列答案
相关题目
5.小明同学分别取20gNaOH固体A、B、C,采用不同方法保存.几天后,A未变质、B部分变质、C全部变质,他将三份固体分别配成溶液并滴入20%的稀硫酸直到正好反应.下列说法正确的是( )
| A. | 几天后,三份固体的质量为:A=B=C | |
| B. | 为控制正好反应,A能用酚酞试液指示,B、C可滴加稀硫酸直到正好不冒气泡 | |
| C. | 正好反应时,消耗稀硫酸的质量由大到小的顺序为:A>B>C | |
| D. | 正好反应时,生成硫酸钠的质量都相等,均为35.5g |
2.鉴别二氧化碳和一氧化碳的方法或试剂,错误的是( )
| A. | 澄清石灰水 | B. | 闻气味 | C. | 石蕊溶液 | D. | 点燃 |
19.金属材料有着广泛的用途.
(1)图1所示用品中,利用金属导电性的是B(填字母序号).
(2)下表是一些金属的熔点数据.

铅锡合金中某种金属的质量分数与合金的熔点有如图2所示的关系,其中横坐标表示的是Sn(填化学式)的质量分数;当合金熔点最低时,合金中铅与锡的质量比为2:3.
(3)新型材料纳米级Fe粉在空气中易自燃,能用作高效催化剂,实验室采用还原法制备纳米级Fe粉,流程如图3:
①铁丝在空气中只能灼成红热、离火变冷,而纳米级Fe粉在空气中易自燃,说明物质燃烧的剧烈程度与药品的状态(可燃物与氧气的接触面积)有关.
②写出Ⅱ中用氢气从FeCl2置换出铁的反应方程式H2+FeCl2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl.
在Ⅱ中通入氮气的目的是排尽空气,防止生成的铁粉被反应.
(4)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较强的金属首先被腐蚀.造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是D.(填编号)
A、银块 B、铜块 C、锡块 D、锌块
(5)用下列试剂探究不同金属与酸反应的速率不同:锌片、铁片、5%盐酸.取质量相等的上述两种金属(表面积相同),分别放入溶质质量分数5%的足量稀盐酸中.
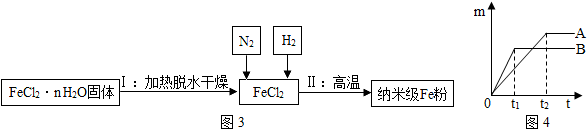
①线B对应的金属是Zn.
②线A对应的金属与稀盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑.
(6)某兴趣小组的同学将一块不纯的铁片5.6g投入到足量的稀盐酸中,充分反应后生成了0.2g气体,则该铁片中混有的杂质一定不可能是D.
A、铝和锌 B、镁和锌 C、镁和铜 D、锌和铜.
(1)图1所示用品中,利用金属导电性的是B(填字母序号).
(2)下表是一些金属的熔点数据.

| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 1083 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
(3)新型材料纳米级Fe粉在空气中易自燃,能用作高效催化剂,实验室采用还原法制备纳米级Fe粉,流程如图3:
①铁丝在空气中只能灼成红热、离火变冷,而纳米级Fe粉在空气中易自燃,说明物质燃烧的剧烈程度与药品的状态(可燃物与氧气的接触面积)有关.
②写出Ⅱ中用氢气从FeCl2置换出铁的反应方程式H2+FeCl2$\frac{\underline{\;高温\;}}{\;}$Fe+2HCl.
在Ⅱ中通入氮气的目的是排尽空气,防止生成的铁粉被反应.
(4)一般情况下,两种活动性不同的金属在潮湿的环境中接触时,活动性较强的金属首先被腐蚀.造船工业为避免轮船的钢铁外壳被腐蚀,通常在轮船外壳镶嵌的金属是D.(填编号)
A、银块 B、铜块 C、锡块 D、锌块
(5)用下列试剂探究不同金属与酸反应的速率不同:锌片、铁片、5%盐酸.取质量相等的上述两种金属(表面积相同),分别放入溶质质量分数5%的足量稀盐酸中.

①线B对应的金属是Zn.
②线A对应的金属与稀盐酸反应的化学方程式Fe+2HCl═FeCl2+H2↑.
(6)某兴趣小组的同学将一块不纯的铁片5.6g投入到足量的稀盐酸中,充分反应后生成了0.2g气体,则该铁片中混有的杂质一定不可能是D.
A、铝和锌 B、镁和锌 C、镁和铜 D、锌和铜.
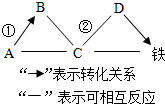 A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种.它们之间的反应或转化关系如图(部分物质和反应条件已略去).则化学方程式:①Ca(OH)2+CO2=CaCO3↓+H2O;②Fe2O3+6HCl=2FeCl3+3H2O;A在生产或生活中的一种用途是改良酸性土壤.
A、B、C、D分别为氧化铁、盐酸、氢氧化钙、碳酸钙中的一种.它们之间的反应或转化关系如图(部分物质和反应条件已略去).则化学方程式:①Ca(OH)2+CO2=CaCO3↓+H2O;②Fe2O3+6HCl=2FeCl3+3H2O;A在生产或生活中的一种用途是改良酸性土壤.