题目内容
13.化学实验室要从含少量铜粉的银、锰(Mn)混合金属粉末中分离出贵金属,并获得一种盐晶体,将有关三种金属随意编号为:A、B、C,并设计了如下流程:
(1)A、B、C三种金属的活动性顺序为A>B>C.
(2)金属C是Ag,操作a的名称是蒸发结晶,在过滤操作时,用到的玻璃仪器有烧杯、漏斗和玻璃棒.
(3)用化学变化方法验证加入的硝酸银溶液是否足量的方法是取少量②后滤渣于试管中加热,冷却后加入足量稀硫酸振荡后静置,若上层清液为蓝色则不足量,若上层清液为无色则硝酸银溶液为足量.
分析 利用金属活动性顺序判断金属是否与酸反应、金属是否能与盐溶液的反应.另外,还得知道结晶是从溶液中得到溶质的一种办法;验证硝酸银溶液可以验证银离子.
解答 解:(1)在金属活动性顺序中,铜、银排在氢的后面,所以不能与酸反应放出氢气,由题意可知三种金属中只有A能与稀硫酸反应生成无色气体和A的盐溶液,所以我们判断A是Mn;金属B、C的混合物加入足量的含硝酸银的回收液中,过滤后得到金属C,说明金属C不能与硝酸银溶液反应,金属B能与硝酸银溶液反应,所以我们得知金属B的活动性大于金属C的活动性,又因为在金属活动性顺序中,铜排在银的前面,所以B是Cu,C是银.故答案为:A B C;
(2)我们得知金属B的活动性大于金属C的活动性,又因为在金属活动性顺序中,铜排在银的前面,所以B是Cu,C是银.要想从A的盐溶液中得到A的硫酸盐晶体,我们可以采用蒸发结晶的办法,用到的玻璃仪器是酒精灯和玻璃棒; 故答案为:Ag;蒸发结晶;漏斗;
(3)取少量②后滤渣于试管中加热,冷却后加入足量稀硫酸振荡后静置,若上层清液为蓝色则不足量,若上层清液为无色则硝酸银溶液为足量.
故答案为:(1)A>B>C (或Mn>Cu>Ag)(2)Ag蒸发结晶,漏斗 (3)取少量②后滤渣于试管中加热,冷却后加入足量稀硫酸振荡后静置,若上层清液为蓝色则不足量,若上层清液为无色则硝酸银溶液为足量.
点评 此题以实验设计流程的形式让学生去利用金属活动性顺序表解决有关金属化学性质的问题,有一定的深度和广度.

练习册系列答案
相关题目
18.下列有关粒子的说法不正确的是( )
| A. | 构成物质的粒子有分子、原子、离子 | |
| B. | 最外层电子数达到稳定结构的粒子一定是稀有气体 | |
| C. | 在化学变化中,氯原子容易得到电子变成氯离子 | |
| D. | 相同的原子可能构成不同的分子 |
5.下列物质属于纯净物的是( )
| A. | 空气 | B. | 矿泉水 | C. | 二氧化碳 | D. | 稀有气体 |
5.按体积分数计算,空气中含量最多的气体是( )
| A. | N2 | B. | O2 | C. | CO2 | D. | H2O |
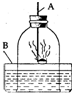 如图是空气中氧气含量的测定装置
如图是空气中氧气含量的测定装置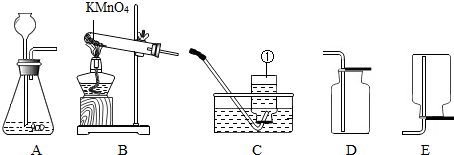
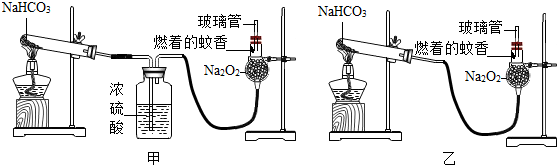
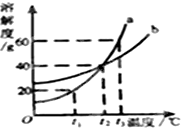 如图为a、b两种固体物质的溶解度曲线,请依据曲线图回答问题:
如图为a、b两种固体物质的溶解度曲线,请依据曲线图回答问题: