题目内容
2.实验是进行科学研究的重要方式.(1)除去粗盐中难容性杂质实验中,主要有四步实验,如图
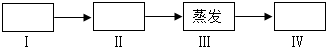
步骤Ⅲ,给蒸发皿加热时不需要(选填“需要”或“不需要”)垫上石棉网;步骤Ⅳ是计算产率.
(2)除去粗盐中难溶性杂质的四步实验中,有四步(填数值)用到了玻璃棒.
(3)该小组下列操作,影响第Ⅳ步结果的是AC.
A.未充分溶解就过滤 B.蒸发时水分未完全蒸干 C.蒸发时盐粒溅出蒸发皿
(4)实验室配制一定量10%的氯化钠溶液(已知水的密度为1g/cm3).
①用8.0g氯化钠固体配制10%的氯化钠溶液,需要水72.0mL.
②在溶液配制过程中,溶解时要用玻璃棒.
③将配好的溶液倒入洁净的细口瓶中(填容器名称),盖好塞子贴上标签.
④溶液配制过程中除了天平、量筒、烧杯、玻璃棒外,还需要用到的仪器药匙、胶头滴管.
⑤下列操作会导致配制的氯化钠溶液的溶质质量分数偏低的是AB.
A.氯化钠固体中含有杂质
B.烧杯未干燥直接用于配制溶液
C.用量筒量取水时采用俯视方法读数.
分析 (1)根据蒸发皿的使用方法和玻璃棒的使用解答;
(2)根据粗盐提纯的影响结果的因素解答;
(3)根据实验误差选择;
(4)根据配制溶质质量分数的步骤、仪器、注意事项解答;
解答 解:(1)蒸发皿是可以直接加热的仪器,粗盐中难容性杂质实验的步骤是溶解、过滤、蒸发、计算产率.
(2)除去粗盐中难溶性杂质的四步实验每一步都用到了玻璃棒;
(3)对产率有影响的操作是氯化钠有损失的错误操作,如未充分溶解就过滤、蒸发时盐粒溅出蒸发皿等;
(4)氯化钠溶液质量=8.0g÷10%=80g,水的质量=80g-8g=72.0g;体积为72.0ml;在溶液配制过程中,溶剂时需要用到玻璃棒,配好的溶液盛放于细口瓶中;溶液配制过程中用到的仪器有天平、量筒、烧杯、玻璃棒、药匙、胶头滴管;导致配制的氯化钠溶液的溶质质量分数偏低的因素有氯化钠固体中含有杂质,烧杯不干燥直接用于配制溶液,用量筒量取水时采用仰视方法读数,药品与砝码位置放反等.
故答案为:(1)不需要 计算产率(2)四(3)AC (4)①72.0 ②溶解 ③细口瓶 ④药匙、胶头滴管 ⑤AB
点评 使用固体溶质配制溶液时,由于既要称取固体溶质的质量又要量取液体溶剂的体积,其操作过程为计算-称量-溶解.

练习册系列答案
相关题目
14.下列过程中不包含化学变化的是( )
| A. | 测铅笔芯的导电性 | |
| B. | 点燃蜡烛,用冷碟子收集碳炭黑 | |
| C. | 用小苏打水、柠檬酸等制汽水 | |
| D. | 用玫瑰花浸出液测氢氧化钠溶液的酸碱性 |
15.下列有关粒子结构示意图的四种说法正确的是( )


| A. | ①②表示的元素在元素周期表中位于同一横行 | |
| B. | ④⑤两种元素的化学性质相似 | |
| C. | ②表示阴离子 | |
| D. | ②⑤表示金属元素的粒子 |
10.下列认识不正确的是( )
| A. | 在书写具有保存价值的档案时,最好使用碳素笔 | |
| B. | 二氧化碳是一种能产生温室效应的气体 | |
| C. | 生铁和钢主要成分都是铁,但它们的含碳量不同 | |
| D. | 铝制品很耐腐蚀,是因为铝的化学性质很稳定 |
7.某同学在化学记录本上有如下记录,你认为不正确的是( )
| A. | 配平化学方程式的依据是质量守恒定律 | |
| B. | 从元素周期表中可以查出元素的相对原子质量 | |
| C. | 用澄清石灰水可鉴别空气、氧气、二氧化碳、氮气四种气体 | |
| D. | 化学反应发生时不一定能观察到明显的现象 |
12.推理是学习化学的重要思维方法,以下推理正确的是( )
| A. | 稀盐酸中能解离出氢离子,硫酸溶液中也能解离出氢离子 | |
| B. | 铝锅表面易形成致密的氧化铝薄膜耐腐蚀,铁制品表面易形成铁锈也耐腐蚀 | |
| C. | 某石灰矿中检测出含有氧化铁,因此该矿石也可用来炼铁 | |
| D. | 碳酸盐与盐酸反应放出气体,所以与盐酸反应放出气体的物质一定是碳酸盐 |

