题目内容
实验室中用10g大理石与足量稀盐酸反应制取二氧化碳,如果制得3.3g二氧化碳,那么大理石中含碳酸钙多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据生成的二氧化碳的质量,由反应的化学方程式计算出大理石中含碳酸钙的质量即可.
解答:解:设大理石中含碳酸钙的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
=
x=7.5g
答:大理石中含碳酸钙的质量为7.5g.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 3.3g
| 100 |
| 44 |
| x |
| 3.3g |
答:大理石中含碳酸钙的质量为7.5g.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
纳米级材料二氧化钛(TiO2)能有效去除因装修带来的多种有害气体.TiO2中Ti的化合价为( )
| A、+1 | B、+2 | C、+4 | D、-4 |
下列实验操作正确的是( )
A、 液体加热 |
B、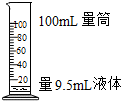 |
C、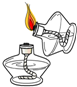 点燃酒精灯 |
D、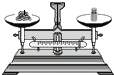 称量10.05g固体 称量10.05g固体 |
如图是元素周期表中的一格,依据图中的信息得到的下列认识中错误的是( )
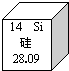

| A、该元素原子的质子数为14 |
| B、该元素属于金属元素 |
| C、该元素的符号是Si |
| D、该元素的相对原子质量为28.09 |