题目内容
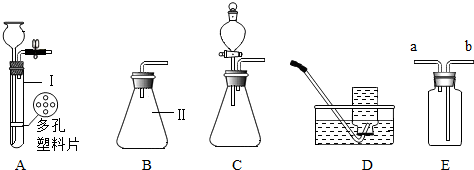
下面是几种实验室制取气体的发生装置和收集装置,请回答下列问题: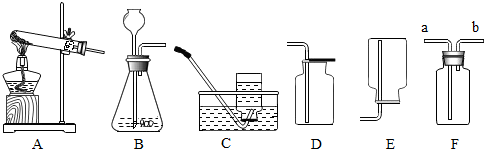
(1)实验室用氯酸钾和二氧化锰制取氧气时应选用 (填字母标号,下同)发生装置.若要收集较为纯净的氧气最好选用 装置,停止加热时,先要把 ,再熄灭酒精灯.
(2)实验室常用锌粒和稀硫酸反应来制取氢气,应选用的发生装置是 ,氢气密度比空气小,不溶于水,可用 装置收集.
(3)装置F是一种可用于集气、洗气等的多功能装置.若将F装置内装满水,再连接量筒,用于测定不溶于水且不与水反应的气体体积,则气体应从 (填“a”或“b”)端进入F中.
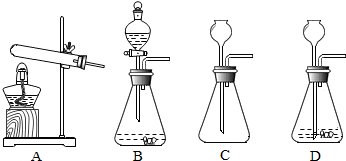
(4)实验室内用块状固体碳化钙和水反应制取乙炔(C2H2)气体,该反应非常激烈且放出大量的热,最适合使用的发生装置是如图中的 .

(1)实验室用氯酸钾和二氧化锰制取氧气时应选用
(2)实验室常用锌粒和稀硫酸反应来制取氢气,应选用的发生装置是
(3)装置F是一种可用于集气、洗气等的多功能装置.若将F装置内装满水,再连接量筒,用于测定不溶于水且不与水反应的气体体积,则气体应从
(4)实验室内用块状固体碳化钙和水反应制取乙炔(C2H2)气体,该反应非常激烈且放出大量的热,最适合使用的发生装置是如图中的

考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,制取氧气的操作步骤和注意点,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)加热氯酸钾制取氧气属于固体加热型,故选发生装置A,并据反应原理书写表达式,收集较为纯净的气体通常用排水法;根据注意事项来分析;
(2)根据反应物的状态和反应条件来确定制取装置,根据气体的性质来确定收集方法;
(3)用排水法收集气体,因为气体的密度都小于液体的密度,必需短进长出;
(4)制取装置包括加热和不需加热两种,用实验室常用块状固体碳化钙与水反应制备乙炔(C2H2),是固体与液体在常温下反应制取气体,因此不需要加热;该反应比二氧化锰催化过氧化氢分解更加剧烈,因此选用有分液漏斗的装置,因为分液漏斗可以控制反应的速度.
(2)根据反应物的状态和反应条件来确定制取装置,根据气体的性质来确定收集方法;
(3)用排水法收集气体,因为气体的密度都小于液体的密度,必需短进长出;
(4)制取装置包括加热和不需加热两种,用实验室常用块状固体碳化钙与水反应制备乙炔(C2H2),是固体与液体在常温下反应制取气体,因此不需要加热;该反应比二氧化锰催化过氧化氢分解更加剧烈,因此选用有分液漏斗的装置,因为分液漏斗可以控制反应的速度.
解答:解:(1)加热氯酸钾制取氧气属于固体加热型,故选发生装置A,氧气不易溶于水,故收集较为纯净的气体可用排水法;实验结束,停止加热时要先把导管移出水面,再熄灭酒精灯,其理由是防止水倒流而炸裂试管;故填:A;C;导管移出水面;
(2)用固体锌和稀硫酸溶液的混合物常温制取氢气,不需加热,故选发生装置B;由氢气难溶于水,所以可用排水法收集,密度比空气小,故可用向下排空气法收集;故填:B;C或E;
(3)由于F装置内装满水,如果气体从a管进入集气瓶,由于气体的密度远小于水的密度,进入集气瓶内的气体会从b管中导出;而从b管进入,由于气体不溶于水,在气体压力的不断增大下,集气瓶中的水会被压出,在另一端连接量筒,通过量筒内水的体积便可测定收集到的气体的体积.故填:b;
(4)A、用实验室常用块状固体碳化钙与水反应制备乙炔(C2H2),是固体与液体在常温下反应制取气体,因此不需要加热,故选项错误;
B、用实验室常用块状固体碳化钙与水反应制备乙炔(C2H2),是固体与液体在常温下反应制取气体,因此不需要加热;该反应比二氧化锰催化过氧化氢分解更加剧烈,因此选用有分液漏斗的装置,因为分液漏斗可以控制反应的速度;故选项正确;
C、装置直接是错误的装置,长颈漏斗的下端应该在液面以下,故选项错误;
D、该反应比二氧化锰催化过氧化氢分解更加剧烈,因此选用有分液漏斗的装置,因为分液漏斗可以控制反应的速度,长颈漏斗不能控制反应的速度,故选项错误;
故选B.
(2)用固体锌和稀硫酸溶液的混合物常温制取氢气,不需加热,故选发生装置B;由氢气难溶于水,所以可用排水法收集,密度比空气小,故可用向下排空气法收集;故填:B;C或E;
(3)由于F装置内装满水,如果气体从a管进入集气瓶,由于气体的密度远小于水的密度,进入集气瓶内的气体会从b管中导出;而从b管进入,由于气体不溶于水,在气体压力的不断增大下,集气瓶中的水会被压出,在另一端连接量筒,通过量筒内水的体积便可测定收集到的气体的体积.故填:b;
(4)A、用实验室常用块状固体碳化钙与水反应制备乙炔(C2H2),是固体与液体在常温下反应制取气体,因此不需要加热,故选项错误;
B、用实验室常用块状固体碳化钙与水反应制备乙炔(C2H2),是固体与液体在常温下反应制取气体,因此不需要加热;该反应比二氧化锰催化过氧化氢分解更加剧烈,因此选用有分液漏斗的装置,因为分液漏斗可以控制反应的速度;故选项正确;
C、装置直接是错误的装置,长颈漏斗的下端应该在液面以下,故选项错误;
D、该反应比二氧化锰催化过氧化氢分解更加剧烈,因此选用有分液漏斗的装置,因为分液漏斗可以控制反应的速度,长颈漏斗不能控制反应的速度,故选项错误;
故选B.
点评:本考点主要考查了气体的制取装置和收集装置的选择,气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
只用石蕊试剂就可将组内的三种溶液鉴别开的是( )
| A、H2SO4、NaOH、NaCl |
| B、KOH、NaOH、HCl |
| C、HCl、HNO3、Ba(OH)2 |
| D、Ba(OH)2、HCl、H2SO4 |
等体积的下列几种水中,加入肥皂水后产生泡沫最多的是( )
| A、井水 | B、海水 | C、雨水 | D、泉水 |
通电分解水一段时间后,可观察到( )
| A、电极上有气泡,两支玻璃管内气体的体积比约为2:1 |
| B、有氢气和氧气生成,且体积比约为1:2 |
| C、与电源正极相连的玻璃中的气体,能够燃烧 |
| D、与电源负极相连的玻璃管中的气体,能使带火星的木条复燃 |
 (等容积、等质量(含瓶塞、导管、燃烧匙及瓶内少量的细砂)的两个装满氧气的集气瓶置于天平作于哦两盘,并调至平衡,然后同时迅速放入点燃的等质量的白磷和木炭(如图所示)使两者充分燃烧后冷却至室温,打开止水夹后,此时的天平 ( )
(等容积、等质量(含瓶塞、导管、燃烧匙及瓶内少量的细砂)的两个装满氧气的集气瓶置于天平作于哦两盘,并调至平衡,然后同时迅速放入点燃的等质量的白磷和木炭(如图所示)使两者充分燃烧后冷却至室温,打开止水夹后,此时的天平 ( )| A、指针偏向左 |
| B、指针偏向右 |
| C、仍处于平衡状态 |
| D、无法判断 |
下列各组中的物质相互转化时,不能通过一步反应完成的是( )
| A、CO与CO2 |
| B、KCl与KNO3 |
| C、NaOH与Na2CO3 |
| D、H2与H2O |