题目内容
8.实验用2.45g的氯酸钾和0.2g的二氧化锰最多可制取多少克的氧气?分析 根据化学方程式计算所要计算的物质的量即可,注意0.2g的二氧化锰与计算无关.注意过程的完整性
解答 解:用2.45g氯酸钾最多可制取(指完全反应)氧气的质量设为x.
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
2.45g x
$\frac{245}{96}$=$\frac{2.45g}{x}$
x=0.96g
答:2.45g氯酸钾最多可得到0.96g氧气.
点评 根据方程式计算反应物或者生成物的质量时,一要注意方程式必须要正确,其次过程中数据使用要正确,避免无效的劳动.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
20.用分子的观点解释下列现象,其中错误的是( )
| A. | 墙内开花墙外香-分子不断地做无规则的运动 | |
| B. | 物体热胀冷缩-温度升高分子体积变大,温度降低分子体积变小 | |
| C. | 白糖在热水中比在冷水中溶得更快-温度升高分子运动速率加快 | |
| D. | 通常状态下,容积20L的钢瓶中可压入3000L氧气-分子间有间隔 |
17.下列说法正确的是( )
| A. | 鱼类能在水中生存,证明氧气易溶于水 | |
| B. | 活性炭具有吸附性,可用于去除冰箱异味 | |
| C. | 液态氨气和氨水均为纯净物 | |
| D. | 氧气能燃烧,可用作火箭燃料的助燃剂 |
18.已知20℃时,将5g某物质完全溶解后,得到20g该物质的溶液.则20℃时,该物质的溶解度为( )
| A. | 25g | B. | 33.3 | C. | 33.3g | D. | 无法计算 |
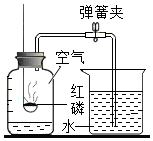 我们已经知道了空气的主要成分是氮气和氧气,如图为测定空气中氧气含量的实验装置图.请回答问题:
我们已经知道了空气的主要成分是氮气和氧气,如图为测定空气中氧气含量的实验装置图.请回答问题: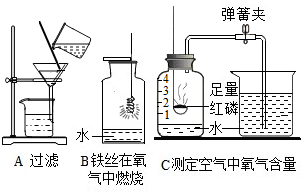 水在实验室中应用也很广泛,水在化学实验中的作用不可忽视.如图中六个实验分别用到水,请回答:
水在实验室中应用也很广泛,水在化学实验中的作用不可忽视.如图中六个实验分别用到水,请回答: