题目内容
1.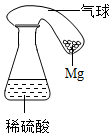 为了探究镁的性质,在锥形瓶(如图)中注入200g质量分数为10%的稀硫酸,在锥形瓶扣紧系一气球,气球内盛有一定量的单质镁碎屑.试根据要求,回答下列问题:
为了探究镁的性质,在锥形瓶(如图)中注入200g质量分数为10%的稀硫酸,在锥形瓶扣紧系一气球,气球内盛有一定量的单质镁碎屑.试根据要求,回答下列问题:(1)将气球内的单质镁全部倒入锥形瓶中.写出中观察到的一项实验现象:气球膨胀起来;
(2)倒入单质镁,反应结束后,整个装置与之前相比较②(填写下列各项的序号).
①没有变化 ②有变化,后者质量变小 ③有变化,后者质量变大 ④不能确定
(3)若稀硫酸完全反应,单质镁仍有剩余,试通过计算,求此时所得不饱和溶液中溶质的质量.(写出相应计算过程,计算结果精确到0.1g)
分析 镁和稀硫酸反应生成硫酸镁和氢气,根据稀硫酸的质量和质量分数可以计算反应生成硫酸镁的质量和生成的氢气质量,进一步可以计算此时所得不饱和溶液中溶质的质量.
解答 解:(1)将气球内的单质镁全部倒入锥形瓶中,能够观察到镁表面产生大量气泡,气球膨胀起来.
故填:气球膨胀起来.
(2)反应结束后,生成了新物质硫酸镁和氢气,又因为气球膨胀起来,产生向上的浮力,称量时质量会变小.
故填:②.
(3)设反应生成的硫酸镁的质量为x,
Mg+H2SO4═MgSO4+H2↑,
98 120
200g×10% x
$\frac{98}{200g×10%}$=$\frac{120}{x}$,
x=24.5g,
答:此时所得不饱和溶液中溶质的质量是24.5g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案
相关题目
11.有关酸碱盐的知识下列说法正确的是( )
| A. | 稀硫酸和氧化铁反应的反应类型属于置换反应 | |
| B. | 100g10%NaOH溶液与100g10%的盐酸充分反应后,溶液呈中性 | |
| C. | 检验自来水中是否含有Cl-时,先加入硝酸银溶液,再加入稀硝酸,如果有白色沉淀出现,则证明溶液中有Cl- | |
| D. | 在农村,人们常取少量化肥和消石灰一起放在手掌心搓,通过闻气味的方法来检验是否是氮肥,因为铵盐和碱反应后有二氧化碳气体生成 |
12.下列区分各物质的两种方案都合理的是( )
| A | B | C | D | |
| 物质 | 碳酸钠和氢氧化钠 | 空气和氧气 | 尿素和硫酸铵 | 木炭和二氧化锰 |
| 方案一 | 稀盐酸 | 带火星的木条 | 加入氢氧化钠溶液 | 加稀盐酸 |
| 方案二 | 酚酞溶液 | 燃烧的木条 | 加水,观察是否潮解 | 观察颜色 |
| A. | A | B. | B | C. | C | D. | D |
10.因汽油价格上调,杭州市区内的士费用外加1元,但这并不意味着机动车的燃料危机已经解除.下列缓解机动车燃料危机的设想不合理的是( )
| A. | 使用乙醇汽油 | |
| B. | 改进发动机的燃烧方式,使汽油充分燃烧 | |
| C. | 从植物中提炼汽油 | |
| D. | 寻找新的催化剂使水变汽油 |
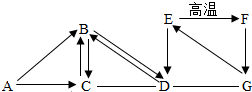 A-G是初中化学常见物质,其中B是单质,D是光合作用的气体原料,G溶液显碱性,如图是这些物质的转化关系,“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略),请回答:
A-G是初中化学常见物质,其中B是单质,D是光合作用的气体原料,G溶液显碱性,如图是这些物质的转化关系,“-”表示相连物质可以发生反应,“→”表示一种物质生成另一种物质(部分反应物、生成物及反应条件省略),请回答: