题目内容
18.实验室配制一定浓度的氯化钠溶液,需要的操作步骤是计算、称量、量取和溶解.(1)配制40g质量分数为10%的氯化钠溶液,所需氯化钠质量为4g.
(2)量取所需蒸馏水要用到的仪器是BC(填字母序号).

(3)若将20g质量分数为10%的氯化钠溶液,稀释为质量分数为4%的氯化钠溶液,需加水的质量是30g.
分析 配制一定质量分数的溶液的步骤:计算、称量(量取)、溶解.
(1)根据溶质质量=溶液质量×溶质的质量分数,进行分析解答.
(2)量取一定量的蒸馏水,应使用量筒.
(3)根据溶液稀释前后,溶质的质量不变,结合题意进行分析解答.
解答 解:实验室配制一定浓度的氯化钠溶液,首先计算配制溶液所需氯化钠和水的质量,再称量所需的氯化钠量取水,最后进行溶解.
(1)溶质质量=溶液质量×溶质的质量分数,配制40g质量分数为10%的氯化钠溶液,所需氯化钠质量为40g×10%=4g.
(2)量取所需蒸馏水,应选择量筒,向量筒内加液时,先用倾倒法加液到近刻度线,再改用胶头滴管加液到刻度线,用到的仪器是量筒和胶头滴管.
(3)设要加水的质量为x,根据溶液稀释前后,溶质的质量不变,
则20g×10%=(20g+x)×4% x=30g.
故答案为:溶解;(1)4;(2)BC;(3)30.
点评 本题难度不大,明确配制一定溶质质量分数的溶液实验步骤、溶质质量=溶液质量×溶质的质量分数、溶液稀释前后溶质的质量不变等是正确解答本题的关键.

练习册系列答案
 寒假创新型自主学习第三学期寒假衔接系列答案
寒假创新型自主学习第三学期寒假衔接系列答案
相关题目
8.往白醋中加入紫色石蕊试剂,石蕊试剂的颜色变为( )
| A. | 无色 | B. | 红色 | C. | 蓝色 | D. | 紫色 |
9.空气是一种宝贵的自然资源,下列说法中错误的是( )
| A. | 空气是混合物 | |
| B. | 空气中氧气的体积分数约为78% | |
| C. | 空气中含有水蒸气 | |
| D. | 氮气化学性质不活泼,可用于食品防腐 |
13.下列物质中,属于氧化物的是( )
| A. | O2 | B. | Al2O3 | C. | Na2CO3 | D. | H2SO4 |
10.下列属于化学变化的是( )
| A. | 冰雪融化 | B. | 铁锅生锈 | C. | 香水挥发 | D. | 矿石粉碎 |
7.某研究性学习小组的同学对实验室里久置于空气中变质的过氧化钠(Na2O2)固体的成分进行探究.
【查阅资料】
(1)Na2O2化学性质很活泼,能与水、二氧化碳反应,相关化学方程式为:2Na2O2+2H2O=4NaOH+O2↑; 2Na2O2+2CO2=2Na2CO3+O2.
(2)Na2CO3溶液与中性的CaCl2溶液能发生复分解反应.
【猜想】
Ⅰ:固体为Na2O2、NaOH、Na2CO3的混合物
Ⅱ:固体为NaOH和Na2CO3的混合物
Ⅲ:固体为NaOH
Ⅳ:固体为Na2CO3
【实验探究】
【反思评价】固体Na2O2应密封保存.
【查阅资料】
(1)Na2O2化学性质很活泼,能与水、二氧化碳反应,相关化学方程式为:2Na2O2+2H2O=4NaOH+O2↑; 2Na2O2+2CO2=2Na2CO3+O2.
(2)Na2CO3溶液与中性的CaCl2溶液能发生复分解反应.
【猜想】
Ⅰ:固体为Na2O2、NaOH、Na2CO3的混合物
Ⅱ:固体为NaOH和Na2CO3的混合物
Ⅲ:固体为NaOH
Ⅳ:固体为Na2CO3
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体于试管中,加水振荡,直至完全溶解. | 无气泡产生 | 猜想 I不成立 |
| ②取少量①中的溶液于试管中,滴加CaCl2溶液. | 有白色沉淀产生 | 证明有Na2CO3存在 |
| ③ 取少量①中的溶液于试管中,加入过量CaCl2溶液使沉淀完全,静置后,向上层清液中滴加酚酞试液 | 酚酞试液变红 | 证明有NaOH存在 |
综合以上实验现象,说明猜想II是成立的. | ||
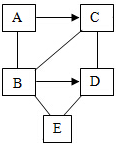 ABCDE是初中化学常见的不同类别的物质,其中A是铁锈的主要成分,D物质的溶液呈蓝色,C分别与B、D反应有一种产物相同,“→”表示一种物质转化为另一种物质,“--”表示两端物质一定条件下可以发生反应(反应条件、部分反应物和生成物略去),请回答下列问题:
ABCDE是初中化学常见的不同类别的物质,其中A是铁锈的主要成分,D物质的溶液呈蓝色,C分别与B、D反应有一种产物相同,“→”表示一种物质转化为另一种物质,“--”表示两端物质一定条件下可以发生反应(反应条件、部分反应物和生成物略去),请回答下列问题: