题目内容
12. 淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状,提出问题并在实验室进行了以下探究.
淡水资源的缺乏已成为制约社会发展的重要因素,从浩瀚的海洋里获取淡水,对解决淡水危机具有重要意义.某小组针对这一现状,提出问题并在实验室进行了以下探究.【提出问题】如何从海水中获取淡水?
【实验用品】酒精灯、试管、单孔橡皮塞、玻璃导管、铁架台、烧杯、胶头滴管、海水、硝酸银溶液.
【实验过程】
①如图组装仪器并检查装置气密性.
②向大试管加入5~10mL海水,塞好橡皮塞,用酒精灯加热.加热一段时间后,小试管内收集到很少液体,试管口有大量白雾.
该小组同学建议对该装置进行改进,你认为改进的措施为:把小试管浸在冷水中.
③向小试管里的冷凝水中滴加几滴硝酸银溶液,现象为:无明显现象.
【得出结论】
通过上述实验探究,你得出的结论是:蒸发海水可以获得淡水.
【反思交流】
①对海水淡化后剩余资源,请提出一种合理利用的措施:获取食盐.
②“蒸馏法淡化海水”的思路是想办法将水从混合物中分离出来.请列举一种与上述原理相同的混合物分离的例子:石油分馏获取汽油、柴油.
分析 在温度比较低的环境中有利于水蒸气的冷凝;
氯离子能和银离子结合生成白色沉淀氯化银;
海水淡化后剩余资源中含有大量的氯化钠;
利用沸点不同,通过石油分馏可以获取汽油、柴油等.
解答 解:【提出问题】如何从海水中获取淡水.
故填:如何从海水中获取淡水?
【实验过程】
温度较高时不利于水蒸气液化,为了使水蒸气尽快液化,应该把小试管浸在冷水中,因此改进的措施是把小试管浸在冷水中.
故填:把小试管浸在冷水中.
向小试管里的冷凝水中滴加几滴硝酸银溶液,由于冷凝水中不含有氯离子,因此无明显现象.
故填:无明显现象.
【得出结论】
通过上述实验探究,得出的结论是蒸发海水可以获得淡水.
故填:蒸发海水可以获得淡水.
【反思交流】
①对海水淡化后剩余资源,可以用来获取食盐.
故填:获取食盐.
②“蒸馏法淡化海水”的思路是想办法将水从混合物中分离出来,与上述原理相同的混合物分离的例子是石油分馏获取汽油、柴油.
故填:石油分馏获取汽油、柴油;分离液态空气(其它合理答案均得分)
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
2.某溶液中含有硝酸银、硝酸铜和硝酸钡三种溶质,现有三种试剂:①NaOH溶液、②NaCl溶液、③Na2CO3溶液,若每加一种试剂只生成一种沉淀,则所加试剂的先后顺序是( )
| A. | ①②③ | B. | ②③① | C. | ②①③ | D. | ③②① |
3.下列物质中含有氧气的是( )
| A. | 过氧化氢 | B. | 二氧化锰 | C. | 二氧化碳 | D. | 空气 |
7.小明发现一种淡黄色的粉末可以用于杀菌、消毒和漂白,于是想探究该固体的成分.
[提出问题]该淡黄色固体的化学成分是什么?
[查阅资料]
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
[设计实验方案]
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是方案一,理由是操作简单,现象明显,对环境无污染.(从环保、操作等角度分析)
[实验验证并得出结论]
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.
小明想对生成的气体成分判断,他提出了以下两种假设:
①该气体是CO ②该气体是O2
你认为上述假设哪个更合理?并说明选择的理由.假设②合理,因为化学反应前后元素种类不变,反应物中不含碳元素
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论).
[计算]在过氧化钠(Na2O2)中,①氧元素的化合价为-1;
②过氧化钠中钠、氧元素的质量比为23:16.
[提出问题]该淡黄色固体的化学成分是什么?
[查阅资料]
(1)硫单质是一种淡黄色固体,难溶于水,在空气中点燃硫单质,生成一种无色、有刺激性气味的气体.
(2)过氧化钠(Na2O2)是一种淡黄色固体,能与水反应,生成气体并放出大量的热.
[设计实验方案]
方案一:取少量该固体粉末于试管中,加2mL水,振荡并观察现象.
方案二:在燃烧匙里放少量该固体,在酒精灯上加热,观察现象.
比较以上两方案,你认为的最佳方案是方案一,理由是操作简单,现象明显,对环境无污染.(从环保、操作等角度分析)
[实验验证并得出结论]
小明向盛有少量该固体的试管中加入2mL水,立刻观察到有无色气泡产生,并且验证出该反应同时生成了氢氧化钠(NaOH).通过实验验证,确定该淡黄色粉末为过氧化钠.
小明想对生成的气体成分判断,他提出了以下两种假设:
①该气体是CO ②该气体是O2
你认为上述假设哪个更合理?并说明选择的理由.假设②合理,因为化学反应前后元素种类不变,反应物中不含碳元素
请设计一个实验,验证你的合理假设(写出简要操作步骤、实验现象和结论).
| 操作步骤 | 实验现象 | 结论 |
②过氧化钠中钠、氧元素的质量比为23:16.
17.化学兴趣小组的同学在报纸上看到这样一则新闻报道:《成都一大货车载电石狂奔燃烧 火龙震撼 仿佛好莱坞大片》某日凌晨2点50分左右,一辆满载20吨电石的挂车,在成南高速路上燃起熊熊大火,黑烟如蘑菇升空,不时发出“嘭嘭”爆炸声.让电石起火的是雨水,电石遇水燃烧爆炸.而雨一直下,燃烧现场一直无法处理.从火灾发生到初步控制住,一共用掉4吨干粉.电石,学名碳化钙(CaC2),是由生石灰和焦炭在电炉中加热到2000℃生成.电石的化学性质非常活泼,遇水就会发生剧烈化学反应,生成一种可燃气体乙炔和一白色固体物质,并放出大量的热.所以,水不能灭这个火,水在其中的角色是助燃!电石起火在正常情况下,可以用磷酸盐干粉、干黄沙和水泥进行覆盖、隔离扑灭,但因为现场雨下得很大,这三种物质无法完全发挥作用,只能就近让它烧光.针对以上新闻内容,大家展开了热烈的讨论:
【讨论与交流】
同学们对于可燃气体乙炔很感兴趣,想通过设计实验来得出乙炔的化学式
查阅资料:
已知乙炔是一可燃性气体,由碳氢元素组成,一个乙炔分子中共有四个原子构成.
实验设计:
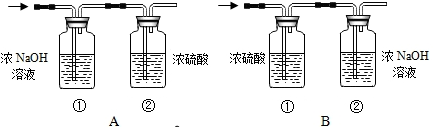
交流讨论:
(1)由于涉及了两套吸收装置,实验小组的两位同学对于上述实验装置A和装置B的选用发生了争执,你认为应该选择B,理由:A装置混合气体通过氢氧化钠,氢氧化钠增重的质量就是二氧化碳;但是也会带一部分水进入浓硫酸,所以浓硫酸增重的质量就不再全部是燃烧的产物水.
实验测定:
经讨论后,他们选定了实验装置,进行实验. 记录数据于下表中
(2)试通过计算,判断乙炔的化学式C2H2,写出计算过程:
【讨论与交流】
同学们对于可燃气体乙炔很感兴趣,想通过设计实验来得出乙炔的化学式
查阅资料:
已知乙炔是一可燃性气体,由碳氢元素组成,一个乙炔分子中共有四个原子构成.
实验设计:

交流讨论:
(1)由于涉及了两套吸收装置,实验小组的两位同学对于上述实验装置A和装置B的选用发生了争执,你认为应该选择B,理由:A装置混合气体通过氢氧化钠,氢氧化钠增重的质量就是二氧化碳;但是也会带一部分水进入浓硫酸,所以浓硫酸增重的质量就不再全部是燃烧的产物水.
实验测定:
经讨论后,他们选定了实验装置,进行实验. 记录数据于下表中
| 装置及质量 | 反应前质量/g | 反应后质量/g |
| 装置① | 125.3 | 127.1 |
| 装置② | 78.2 | 87.0 |
