题目内容
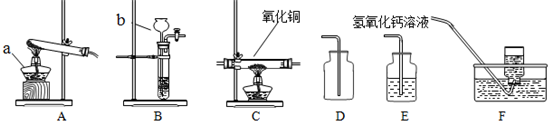
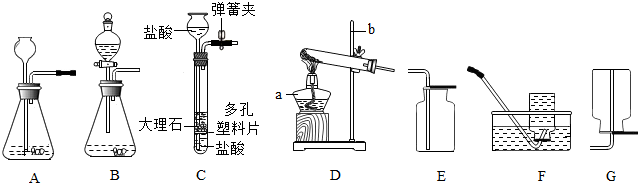
19.下列各组对比实验,能达到实验目的是( )| 实验目的 | 实验方案 | |
| A | 探究燃烧所有条件 |  |
| B | 探究铁生锈所有条件 |  |
| C | 探究食盐和高锰酸钾在水中溶解性 |  |
| D | 实验室制取二氧化碳的药品研究 |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据研究燃烧的条件,应采用两个变量,一是可燃物不一样,再就是隔绝氧气进行解答;
B、根据铁生锈的条件是氧气和水进行解答;
C、根据探究探究食盐和高锰酸钾在水中溶解性只改变溶质的种类其他条件不变进行解答;
D、根据该实验中有两个变量进行解答.
解答 解:A、研究燃烧的条件,应采用两个变量,一是可燃物不一样,再就是隔绝氧气,所以该实验不能探究燃烧的所有条件,故A错误;
B、铁生锈的条件是氧气和水,所以探究铁生锈所有条件,一是只有水看是否生锈,二是只有氧气看是否生锈,三是氧气和水同时存在看是否生锈,故B错误;
C、探究探究食盐和高锰酸钾在水中溶解性只改变溶质的种类其他条件不变,所以可以达到实验目的,故C正确;
D、因为实验中同时改变两个条件,一是所取得酸不同,二是碳酸钙状态不同,所以实验结果没有意义,故D错误.
故选C.
点评 此题主要考查了学生对控制变量法的理解和运用,涉及到了影响反应速率的条件、燃烧的条件和铁生锈所有条件的探究等,属常规性对比试验探究题.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
4.下列实验现象的描述正确的是( )
| A. | 铁在氧气中燃烧生成四氧化三铁 | |
| B. | 磷在氧气中燃烧产生大量的白雾 | |
| C. | 硫在空气中燃烧发出明亮的蓝紫色火焰,生成带刺激性气味的气体 | |
| D. | 木炭在氧气中燃烧,发出白光,放出大量的热 |
11. 如图所示,在装着红棕色二氧化氮气体的瓶子上面,倒扣一个空瓶子,使两个瓶口相对,之间用一块玻璃板隔开.抽出玻璃板后,比空气密度大的二氧化氮进到了上面的瓶子.这个现象说明( )
如图所示,在装着红棕色二氧化氮气体的瓶子上面,倒扣一个空瓶子,使两个瓶口相对,之间用一块玻璃板隔开.抽出玻璃板后,比空气密度大的二氧化氮进到了上面的瓶子.这个现象说明( )
 如图所示,在装着红棕色二氧化氮气体的瓶子上面,倒扣一个空瓶子,使两个瓶口相对,之间用一块玻璃板隔开.抽出玻璃板后,比空气密度大的二氧化氮进到了上面的瓶子.这个现象说明( )
如图所示,在装着红棕色二氧化氮气体的瓶子上面,倒扣一个空瓶子,使两个瓶口相对,之间用一块玻璃板隔开.抽出玻璃板后,比空气密度大的二氧化氮进到了上面的瓶子.这个现象说明( )| A. | 气体分子在不停地运动 | B. | 气体分子之间存在引力和斥力 | ||
| C. | 气体是由分子组成的 | D. | 温度越高,气体分子运动越剧烈 |
9.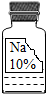 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】(1)根据受损标签判断,这瓶试剂不可能是酸
A.酸 B.碱 C.盐
【查阅资料】Ⅰ.Na2CO3和NaHCO3溶液都呈碱性.Ⅱ.测定室温(20℃)时,四种物质的溶解度的数据如下
得出结论】(2)小华根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是NaHCO3.
【继续探究】(3)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得PH>7,这瓶试剂不可能是NaCl.
(4)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
反思评价】(5)老师指出,即便小强在实验中确实观察到白色沉淀,也不能肯定该溶液一定是碳酸钠溶液.原因是氢氧化钠溶液变质后也会生成碳酸钠.
 实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:
实验室有一瓶保管不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是NaCl、NaOH、Na2CO3、NaHCO3中的一种.小强和小华同学很感兴趣,决定对其成分进行探究:【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】(1)根据受损标签判断,这瓶试剂不可能是酸
A.酸 B.碱 C.盐
【查阅资料】Ⅰ.Na2CO3和NaHCO3溶液都呈碱性.Ⅱ.测定室温(20℃)时,四种物质的溶解度的数据如下
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 21.5 | 9.6 |
【继续探究】(3)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得PH>7,这瓶试剂不可能是NaCl.
(4)小强为了检验该溶液是NaOH溶液还是Na2CO3溶液,他又进行了如下实验:
| 操作步骤 | 实验现象 | 结论及化学方程式 |
| 取样于试管中,滴加 CaCl2溶液[或Ca(OH)2溶液] | 观察到白色沉淀 | 该溶液是Na2CO3溶液 反应的化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl(或Na2CO3+Ca(OH)2═CaCO3↓+2NaOH) |
 如图是“×××”补钙剂商品标签图.我能根据标签信息完成下列问题:
如图是“×××”补钙剂商品标签图.我能根据标签信息完成下列问题: