题目内容
5.按下列实验步骤和要求,回答粗盐提纯的有关问题.第一步:称量、溶解.
在天平上称取5.0g粗盐,用10mL水溶解称取的粗盐(已知5.0g粗盐在10mL水中不能完全溶解).
(1)称量:称量前先把游码移到零刻度处,检查天平的摆动是否平衡,当发现指针偏左时,紧接着的操作是将平衡螺母向右旋,准确称取5.0g粗盐.
(2)溶解:将称取的5.0g粗盐放在烧杯中,再量取10mL水倒入烧杯里,用玻璃棒不断搅拌,直到粗盐不再溶解为止,玻璃棒的作用是加速溶解.若要估算粗盐在10mL水中溶解的克数,还应进行的实验是称量剩余的质量.
第二步:过滤.
(1)待过滤的混合液在引流之前往往要静置一会儿,其目的是使固体杂质沉淀.
(2)过滤时要做到“一贴”、“二低”、“三靠”,“一贴”是滤纸紧贴漏斗内壁.“二低”是①滤纸边缘低于漏斗,②液面低于滤纸边缘.“三靠”是①倾倒液体的烧杯靠玻璃棒,②玻璃棒下端靠三层滤纸,③漏斗下端靠烧杯内壁.
(3)若滤液仍然浑浊,应检查过滤器,再重新过滤.出现浑浊的可能原因是滤纸破损,仪器不洁净,倾倒液体时液面高于滤纸边缘.
第三步:蒸发.
(1)加热蒸发滤液时,要用到的仪器是蒸发皿、酒精灯、带铁圈的铁架台、玻璃棒.
(2)如果蒸发皿中有液滴飞溅,原因是蒸发皿内的液体受热不均,局部过热,应采取的措施是用玻璃棒不断搅拌.
(3)当出现大量晶体时停止加热,利用余热使滤液蒸干,得到纯净的氯化钠晶体.
第四步:转移.
(1)用玻璃棒将固体转移到纸上,称量后,回收到指定容器中.
(2)如果实验温度为20℃,此时100g水中最多溶解氯化钠36g,则理论上可得到纯净的氯化钠3.6g(20℃时,水的密度约为1g/cm3).
分析 第一步称量:要注意天平的使用的要领及方法;估算溶解量就得称量剩余固体的质量.
第二步过滤:的操作应注意玻璃棒的位置以及沉降重复过滤等操作.
第三步蒸发:注意玻璃棒的使用,停火的时间.
第四步转移:同样使用玻璃棒,要注意其使用方法.
解答 解:称量:使用天平,首先要使游码归零,指针向左偏应向右移动螺母.估算粗盐溶解量应称量剩余固体的量.
过滤:一般要注意“一角、二低、三靠”,同时要注意过滤前要先是一部分杂质沉降下来,经反复过滤会使溶液更干净;
蒸发:滤液全部倒入蒸发皿里,加热并不断搅拌,滤液出现大量固体时,停止加热.利用余热烘干精盐,注意不要马上接触蒸发皿,以免烫伤.
转移:使用玻璃棒进行,晾干回收.称取5.0g粗盐,用10mL水溶解称取的粗盐,20℃,此时100g水中最多溶解氯化钠36g,则理论上可得到纯净的氯化钠3.6g.
故答案为:
第一步:
(1)游码移到零刻度处;将平衡螺母向右旋
(2)加速溶解;称量剩余的质量
第二步:(1)使固体杂质沉淀;(2)漏斗内壁;①滤纸边缘低于漏斗;②液面低于滤纸边缘;“三靠”是①倾倒液体的烧杯靠玻璃棒;②玻璃棒下端靠三层滤纸;③漏斗下端靠烧杯内壁 (3)检查过滤器,再重新过滤;滤纸破损,仪器不洁净,倾倒液体时液面高于滤纸边缘.
第三步:(1)蒸发皿,酒精灯,带铁圈的铁架台,玻璃棒;
(2)蒸发皿内的液体受热不均,局部过热;用玻璃棒不断搅拌;(3)出现大量晶体;
第四步:(1)玻璃棒;称量;(2)3.6
点评 在解此类题时,首先要分析各种操作步骤的作用,然后结合选项中的顺序进行分析解答.

练习册系列答案
相关题目
10.黄冈市蕲春县九棵镇是黄冈市经济发展的明星乡镇,其乡镇集团公司下属四家工厂,其中是利用化学原理制造产品的是( )
| A. | 碎石厂(大石块轧成小石子) | B. | 模具厂(钢铁熔化注入模型制成机件) | ||
| C. | 酿酒厂(稻谷酿成酒) | D. | 家具厂(木材加工成家具) |
14.下列物质在盛有空气的密闭容器中燃烧,能除去氧气得到较为纯净的氮气的是( )
| A. | 木炭 | B. | 细铁丝 | C. | 红磷 | D. | 石蜡 |
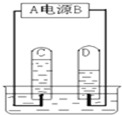 如图为某同学进行电解水实验的装置图,据此回答:
如图为某同学进行电解水实验的装置图,据此回答: