题目内容
2.小丽同学欲通过实验证明“红砖粉末可作过氧化氢分解的催化剂”这一命题.她设计并完成了下列探究:实验一:取5mL水置于试管中,伸入带火星的木条,现象:带火星的木条不复燃.
实验二:取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条,现象:有气泡产生,木条不复燃.
实验三:向5mL5%的过氧化氢溶液中加入红砖粉末,伸入带火星的木条,现象:木条复燃,证明红砖粉末可作催化剂.
分析:(1)在探究中,“实验一”和“实验二”起的作用是对比.
(2)小丽认为仅由上述实验还不能完全得出结论,她补充设计了两个方面的探究,最终完成了对“命题”的实验证明.
第一方面的操作中包含了两次称量,其目的是:比较红砖粉在过氧化氢分解前后的质量是否改变.
第二方面的是利用“实验三”反应后试管内-的剩余物继续实验.接下来的操作是、现象、结论是:
倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明红砖粉仍然能加快过氧化氢的分解.
分析 在验证红砖粉的催化作用时,可设计对比实验,利用对比实验说明红砖粉能加快反应的速度,且反应前后二氧化锰的质量的化学性质保持不变.
解答 解:实验一:水不会产生氧气,不能使带火星的木条复燃;故填:带火星的木条不复燃;
实验三:由题意可知,红砖粉可用作催化剂,那么向5mL5%的过氧化氢溶液中加入红砖粉末,伸入带火星的木条后会发现木条复燃;故填:木条复燃;
【分析】(1)由两个实验的设计可以看出是对比实验.故填:对比;
(2)根据催化剂的特点:“一变,两不变”即能改变化学反应的速率,而本身的质量和化学性质不变;可知
第一方面的实验操作中两次称量,其目的是:比较红砖粉在过氧化氢分解前后的质量是否改变;
第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验.接下来的实验操作、现象和结论是:倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明红砖粉仍然能加快过氧化氢的分解;
故填:比较红砖粉在过氧化氢分解前后的质量是否改变;倾倒掉反应后的液体,向剩余的固体中重新加入过氧化氢溶液,有大量气泡产生,说明红砖粉仍然能加快过氧化氢的分解.
点评 在确定一种物质是催化剂时,不但要确定它能否改变化学反应的速率,还要确定它反应前后的质量和化学性质是否改变.只有这两条都不变,才是催化剂.

练习册系列答案
 阶梯计算系列答案
阶梯计算系列答案
相关题目
13.下列关于微观粒子的说法中不正确的是( )
| A. | 分子是由原子构成的 | B. | 原子中的粒子都不带电 | ||
| C. | 离子是都带电 | D. | 物质不一定是由同种分子构成的 |
10.用适当的数字和符号填空:
氯化钠NaCl;2个镁原子2Mg;5个水分子5H2O;氧化镁中镁元素的化合价为+2$\stackrel{+2}{Mg}$O;
硫酸根离子SO42-,n个亚铁离子nFe2+.
氯化钠NaCl;2个镁原子2Mg;5个水分子5H2O;氧化镁中镁元素的化合价为+2$\stackrel{+2}{Mg}$O;
硫酸根离子SO42-,n个亚铁离子nFe2+.
7.下列各组物质的溶液,只需组内物质相互反应,就能区别的是( )
| A. | Cu(NO3)2 Na2SO4 MgCl2 HCl | B. | BaCl2 K2SO4 Na2CO3 KOH | ||
| C. | FeCl3 HNO3 NaCl NaOH | D. | H2SO4 KCl ZnCl2 CuCl2 |
14.检验集气瓶中是否收集满二氧化碳的方法是( )
| A. | 将燃着的木条放在集气瓶口 | B. | 将燃着的木条伸人集气瓶内 | ||
| C. | 将石灰水倒入集气瓶中 | D. | 将紫色石蕊试液倒人集气瓶中 |
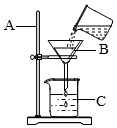 如图所示是某学生设计的过滤操作装置图.
如图所示是某学生设计的过滤操作装置图.