题目内容
14.工业上采用氨碱法生产纯碱(NaCO3),主要流程如图1: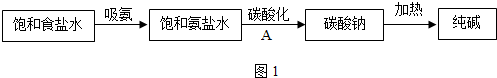
(1)试剂A是CO2,写出通入A步骤反应的化学方程式:NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl.
(2)为什么要先吸氨,后碳酸化?因为饱和氨盐水显碱性,比饱和食盐水更容易吸收二氧化碳,增大二氧化碳的吸收量.
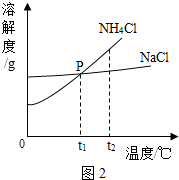
(2)我国化学家侯德榜在氨碱法的基础上创立的“侯氏制碱法”,保留了氨碱法的优点,克服其缺点,即向滤出NaHCO3晶体后的NH4Cl溶液中加入NaCl粉末,析出可用作肥料的NH4Cl,NaCl溶液则可循环使用.NH4Cl和NaCl的溶解度曲线如图2所示.
①二者中氯化铵的溶解度随温度的变化较大.
②将一定量t2℃时NH4Cl饱和溶液的温度降到t1℃,该过程没有发生改变的是C(从下列选项中选择)
A、溶液的质量 B、溶质的质量 C、溶剂的质量 D、溶质质量分数
③要使NH4Cl结晶析出而NaCl留在溶液中,通常将温度控制在较低范围(<t1℃),请说明理由在较低温度下,氯化铵的溶解度小于氯化钠的溶解度,易结晶析出.
④NH4Cl可用作氮肥,在使用时应注意不能与熟石灰混合施用的原因是(用化学方程式表示)2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O.
分析 (1)根据制备的原理来分析;
(2)氨盐水显碱性,容易吸收二氧化碳;
(3)①根据溶解度曲线的意义来分析;
②根据饱和溶液降温后析出晶体来分析;
③根据溶解度曲线来分析;
④根据铵盐遇碱会放出氨气,使化肥肥效降低来分析.
解答 解:(1)向饱和的氨盐水中通入二氧化碳,则氯化钠、水、氨气和二氧化碳反应生成碳酸氢钠和氯化铵,故填:CO2;NH3+CO2+H2O+NaCl═NaHCO3+NH4Cl;
(2)因为饱和氨盐水显碱性,比饱和食盐水更容易吸收二氧化碳,所以在用氨碱法生产纯碱过程中,要先向饱和食盐水中通入氨气,制成饱和氨盐水,再向其中通入二氧化碳.故填:因为饱和氨盐水显碱性,比饱和食盐水更容易吸收二氧化碳,增大二氧化碳的吸收量;
(3)①由溶解度曲线可知,氯化铵的溶解度受温度影响比较大;故填:氯化铵;
②因为氯化铵的溶解度随着温度的降低而减小,所以一定量t2℃时NH4Cl饱和溶液的温度降到t1℃,会析出晶体,溶液的质量会减小,溶质的质量会减小,溶质的质量分数会减小,而溶剂的质量不变,故填:C;
③由溶解度曲线可知,当温度小于t1℃时,氯化铵的溶解度小于了氯化钠的溶解度,氯化铵易结晶析出,故填:在较低温度下,氯化铵的溶解度小于氯化钠的溶解度,易结晶析出;
④氯化铵与氢氧化钙反应生成氯化钙、水和氨气,造成肥效降低;故填:2NH4Cl+Ca(OH)2═CaCl2+2NH3↑+2H2O.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
12.下列对实验现象的描述正确的是( )
| A. | 向加碘食盐溶液中滴加淀粉,溶液不变色 | |
| B. | 铁在氧气中燃烧,火星四射,生成白色固体 | |
| C. | 磷在空气中燃烧,产生大量白烟 | |
| D. | 将50.0mL酒精与50.0mL蒸馏水混合,所得溶液的体积为100.0mL |
2.在生活中,下列做法不正确的是( )
| A. | 通常铝制品很耐腐蚀,清洗时不宜用钢刷、沙等来擦洗 | |
| B. | 为了保护金属资源,目前已经广泛用塑料来代替钢和其他合金制造管道、齿轮和汽车零部件等 | |
| C. | 粉刷墙壁用的乳胶漆是悬浊液 | |
| D. | 把水喷向空中,可以增加养鱼池水中氧气的溶解量 |
6.下列关于元素、原子的说法错误的是( )
| A. | 决定元素的种类是原子的核电荷数 | |
| B. | 原子的最外层电子决定了元素的化学性质 | |
| C. | 原子的质量是由核内质子数与中子数决定的 | |
| D. | 最外层电子数为8的粒子一定是稀有气体的原子 |
 化学小组同学设计了下列兴趣实验.
化学小组同学设计了下列兴趣实验.