题目内容
2.现有碳酸钠和氯化钠的混合物11.1g和50g稀盐酸恰好完全反应,反应完毕后溶液质量为58.9g.求:
(1)原混合物中碳酸钠的质量.
(2)反应后所得溶液中溶质质量分数.(保留到小数点后面一位)
分析 (1)根据质量守恒定律计算生成二氧化碳气体的质量,二氧化碳的质量计算参加反应碳酸钠的质量进行解答;
(2)根据二氧化碳的质量求出生成氯化钠的质量,进而求出反应后所得溶液中溶质质量分数即可.
解答 解:(1)设碳酸钠的质量为x,生成氯化钠的质量为y.
碳酸钠和盐酸反应生成二氧化碳,所以二氧化碳的质量为:50g+11.1g-58.9g=2.2g;
Na2CO3 +2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 2.2g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{2.2g}$
x=5.3g
y=5.85g
(2)反应后所得溶液中溶质质量分数=$\frac{11.1g-5.3g+5.85g}{58.9g}×100%$=19.8%
答:(1)原混合物中碳酸钠的质量为5.3g.
(2)反应后所得溶液中溶质质量分数为19.8%.
点评 本题主要考查了根据化学方程式的计算,了解所得溶液中溶质包括固体中原有的氯化钠和生成的氯化钠是解题的关键,也可利用差量法来解答.

练习册系列答案
 期末好成绩系列答案
期末好成绩系列答案 99加1领先期末特训卷系列答案
99加1领先期末特训卷系列答案 百强名校期末冲刺100分系列答案
百强名校期末冲刺100分系列答案 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
5.试管是初中实验中最常见的仪器,试管口的朝向不同,在实验中的应用也不同.下列有关说法错误的是( )
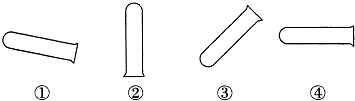

| A. | ①的放置方向,是在加热固体时 | |
| B. | ②的放置方向,是在试管刷洗后 | |
| C. | ③的放置方向,是在加热少量液体时 | |
| D. | ④的放置方向,是向试管里倾倒液体时 |
12.人类的牙齿由一层称为碱式磷酸钙(又名羟基磷酸钙)的坚硬物质保护着,它的化学式中除了钙离子外,还有氢氧根离子和磷酸根离子,则其化学式为( )
| A. | Ca(OH)2(PO4)3 | B. | Ca2(OH)2(PO4)3 | C. | Ca3(OH)2(PO4)3 | D. | Ca5(OH)(PO4)3 |
9.物质发生化学反应时,肯定有变化的是( )
| A. | 原子的数目 | B. | 物质的质量之和 | C. | 分子种类 | D. | 元素种类 |
 某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.
某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功.