题目内容
4.249.5g稀盐酸加入盛有50g碳酸钙的烧杯中,恰好完全反应.试计算:(1)生成二氧化碳的质量;
(2)生成氯化钙的质量;
(3)反应后所得溶液中溶质的质量分数.
分析 碳酸钙玉稀盐酸反应生成氯化钙、水和二氧化碳,由参加反应的碳酸钙的质量,由反应的化学方程式列式计算出生成二氧化碳的质量、生成氯化钙的质量,进而计算出反应后所得溶液中溶质的质量分数.
解答 解:设生成二氧化碳的质量为x,生成氯化钙的质量为y
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 111 44
50g y x
(1)$\frac{100}{44}=\frac{50g}{x}$ x=22g
(2)$\frac{100}{111}=\frac{50g}{y}$ y=55.5g
(3)反应后所得溶液中溶质的质量分数为$\frac{55.5g}{249.5g+50g-22g}$×100%=20%.
答:(1)生成二氧化碳的质量位22g;
(2)生成氯化钙的质量为55.5g;
(3)反应后所得溶液中溶质的质量分数为20%.
点评 本题难度不大,掌握利用化学方程式与溶质质量分数的综合计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
15.下列方程式书写正确的是( )
| A. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | B. | Fe+CuSO4═FeSO4+Cu | ||
| C. | H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+O2↑ | D. | Mg+O2$\frac{\underline{\;点燃\;}}{\;}$MgO2 |
12.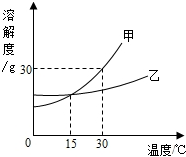 如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
 如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )
如图是甲、乙两种物质的溶解度曲线,下列说法正确的是( )| A. | 甲的溶解度受温度影响比乙小 | |
| B. | 升高温度可使接近饱和的甲溶液变为饱和 | |
| C. | 30℃时乙的溶解度为30g | |
| D. | 15℃时甲、乙的溶解度相等 |
19.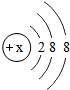 有几种元素的微粒的最外电子层结构如图所示,其中:
有几种元素的微粒的最外电子层结构如图所示,其中:
(1)某电中性微粒一般不和其他元素的原子反应,这种微粒符号是Ar.
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符号是Cl-.
 有几种元素的微粒的最外电子层结构如图所示,其中:
有几种元素的微粒的最外电子层结构如图所示,其中:(1)某电中性微粒一般不和其他元素的原子反应,这种微粒符号是Ar.
(2)某微粒的盐溶液,加入AgNO3溶液时会出现白色浑浊,这种微粒符号是Cl-.
11.世界万物都在变化.如图所示的变化属于化学变化的是 ( )
| A. |  湿衣服晾干 | B. |  带火星木条复燃 | C. |  食盐水的蒸发 | D. |  灯泡通电发光 |