题目内容
12. 研究和控制化学反应条件有重要意义.
研究和控制化学反应条件有重要意义.(1)同学们想探究双氧水的溶质质量分数对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集对间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |
②实验3中,加入的二氧化锰质量为5g.
③相同条件下,实验3产生氧气的速率最快,说明反应物质量分数越大,反应速率越快.
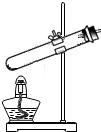
(2)通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择如图装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气.同学们分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
分析 通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气;
根据实验现象可以判断相关方面的问题;
加热时,水容易挥发出较多的水蒸气.
解答 解:(1)①过氧化氢在二氧化锰催化作用下分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
②实验3中,为了进行对比,加入的二氧化锰质量为5g.
故填:5.
③相同条件下,实验3产生氧气的速率最快,说明反应物质量分数越大,反应速率越快.
故填:反应物质量分数越大,反应速率越快.
(2)选择如图装置(气密性良好)进行实验,实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是:加热时水蒸发加快,氧气中混有较多的水蒸气;
同学们分析原因后,采用了排水法收集气体,再检验,证明加热双氧水也可产生氧气.
故填:氧气中混有较多的水蒸气;排水.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
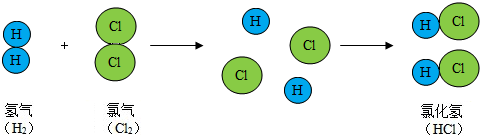
3.如图是氢气与氯气反应生成氯化氢的示意图.下列关于从此图中获取的信息的描述不对的是( )

| A. | 原子不能构成物质,只有分子才是构成物质的基本粒子 | |
| B. | 原子是化学反应中的最小粒子 | |
| C. | 化学反应前后元素的种类不变 | |
| D. | 分子在化学反应中可分裂成原子 |
20.乙酸乙酯(C4H8O2)是一种有浓郁香味,不易溶于水的油状液体,常用作食品、饮料的调香剂.下列有关乙酸乙酯的叙述正确的是( )
| A. | 乙酸乙酯旨中有14个原子 | |
| B. | 乙酸乙酯中碳元素的质量分数为41.4% | |
| C. | 乙酸乙酯中碳、氢元素的质量比为6:1 | |
| D. | “有浓郁香味,不易溶于水”是乙酸乙酯的化学性质 |
7.请用化学符号表示:
(1)2个镁离子:2Mg2+;
(2)地壳中含量最多的金属元素Al;
(3)3个氢氧根离子3OH-;
(4)一氧化氮中氮元素的化合价为+2价$\stackrel{+2}{N}$O.
(1)2个镁离子:2Mg2+;
(2)地壳中含量最多的金属元素Al;
(3)3个氢氧根离子3OH-;
(4)一氧化氮中氮元素的化合价为+2价$\stackrel{+2}{N}$O.
17.下列化学用语与含义不相符的是( )
| A. | 3H--3个氢元素 | B. | O2--氧离子 | ||
| C. | Al2O3--氧化铝 | D. | 2N2--2个氮气分子 |
2.在20℃时,20g水中最多能溶解15gX物质;40℃时,50g水中最多能溶解30gY物质,则X和Y两种物质的溶解度关系式( )
| A. | X>Y | B. | X<Y | C. | X=Y | D. | 无法确定 |
 元素周期表是学习和研究化学的重要工具.回答下列问题:
元素周期表是学习和研究化学的重要工具.回答下列问题: ,氟原子在化学反应中易得到(填“得到”或“失去”)电子,
,氟原子在化学反应中易得到(填“得到”或“失去”)电子,