题目内容
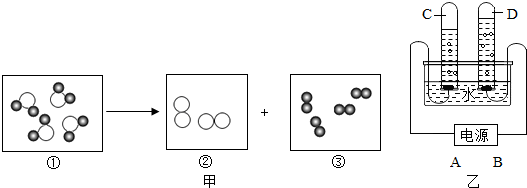
10.写出下列化学反应方程式,并指出其基本反应类型(1)电 解 水2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,分解反应.
(2)氢气在空气中燃烧2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,化合反应.
(3)实验室制取氢气Zn+H2SO4═ZnSO4+H2↑,置换反应.
(4)氢气还原氧化铜CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,置换反应.
(5)不纯氢气点燃爆炸2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,化合反应.
(6)白 磷 自燃4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,化合反应.
分析 电解水生成氢气和氧气;
氢气在空气中燃烧生成水;
通常情况下,锌和稀硫酸反应生成硫酸锌和氢气,氢气难溶于水,密度比空气小;
加热条件下,氧化铜和氢气反应生成铜和水;
不纯氢气点燃爆炸时,氢气和氧气反应生成水;
白磷自燃生成五氧化二磷.
解答 解:(1)电解水的化学方程式为:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,属于分解反应;
(2)氢气在空气中燃烧的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,化合反应,属于化合反应;
(3)实验室制取氢气的化学方程式为:Zn+H2SO4═ZnSO4+H2↑,属于置换反应;
(4)氢气还原氧化铜的化学方程式为:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,属于置换反应;
(5)不纯氢气点燃爆炸的化学方程式为:2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,属于化合反应;
(6)白磷自燃的化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,属于化合反应.
故填:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,分解反应;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,化合反应,化合反应;Zn+H2SO4═ZnSO4+H2↑,置换反应;
CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,置换反应;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O,化合反应;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,化合反应.
点评 书写化学方程式要注意四步:一是反应物和生成物的化学式要正确;二是要遵循质量守恒定律,即配平;三是要有必要的条件;四是看是否需要“↑”或“↓”.

| 甲 | 乙 | 丙 | |
| 加入氢氧化钠溶液质量 (g) | 70 | 80 | 90 |
| 反应得到沉淀的质量 (g) | 5 | 5.8 | 5.8 |
(1)上述实验中,丙同学所用的氢氧化钠溶液一定过量.
(2)求样品中氯化镁的质量(写出计算过程).$\frac{10g-9.5g+11.7g}{50g+80g-5.8g}$
(3)计算乙同学实验后所得溶液中的氯化钠的质量分数.(结果精确到0.01%)
| A. | 绿色植物的花粉 | B. | 火山爆发出的火山灰 | ||
| C. | 光合作用产生的氧气 | D. | 森林大火产生的灰尘 |
问题一、海水制镁过程中如何富集镁离子?
甲、乙、丙三位同学各自提出自己的设想:
甲:直接往海水中加入石灰乳.
乙:高温加热蒸发海水后,加入石灰乳.
丙:向晒盐后的卤水中,加入石灰乳.
通过分析比较,你认为丙的设想最为经济合理(选填“甲”、“乙”或“丙”).
问题二、粗盐纯化过程中如何除去可溶性杂质?
粗盐中含有硫酸钠、氯化钙等杂质.提纯时,先向粗盐水中加过量的氢氧化钡溶液,目的是完全除尽硫酸根离子;再加过量的碳酸钠溶液,除去杂质阳离子;滤去沉淀,向滤液中加入稀盐酸,将溶液的pH调为7,即得到精盐水.
问题三、海水“制碱”的产物成分是什么?
同学们从某企业取回少量碳酸氢钠受热完全分解后的固体样品,为确定其成分,进行了如下探究:
【提出猜想】
甲的猜想:样品中只含有碳酸钠;
乙的猜想:样品中含有碳酸钠和氢氧化钠;
丙的猜想:样品中只含有氢氧化钠.
他们做出上述三种猜想的科学依据是化学反应前后元素的种类不变.
【实验、记录与分析】
| 步骤 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量样品于试管中,加水完全溶解,再加入过量氯化钡溶液; | 生成白色的沉淀 | 丙的猜想不成立 |
| 2 | 取步骤1反应后的溶液与试管中滴加无色的酚酞试液 | 无明显现象 | 只有甲的猜想成立 |
| A. | 缺乏氧气 | |
| B. | 火柴棍的着火点升高了 | |
| C. | 缺乏可燃物 | |
| D. | 燃烧端下方的火柴棍温度不易达到着火点 |
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子.
”表示氧原子.