题目内容
5.氯化钡是一种可溶性重金属盐,广泛应用于化工领域,用毒重石(主要成分为BaCO3)制备氯化钡晶体的工艺流程如图所示: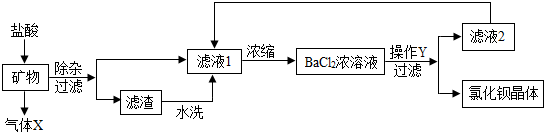
(1)毒重石要进行粉碎的目的是增大反应物的接触面积,加快反应速率;气体X的化学式为CO2.
(2)滤渣是废弃物,若是用碳酸钠溶液检验滤渣是否洗净,则该反应的化学方程式为BaCl2+Na2CO3═BaCO3↓+2NaCl;试剂若是用硝酸银溶液,则可能生成的沉淀的化学式为AgCl,其直接来源可能有2个.
(3)操作Y的名称是降温结晶,滤液2中可循环利用的物质除水外还有BaCl2.
(4)洗涤氯化钡制品最适宜的洗涤剂是C(选填字母).
A.30℃水 B.30℃饱和氯化钠溶液 C.30℃饱和氯化钡溶液.
分析 (1)反应物接触面积越大,反应速率越快;
碳酸钡和稀盐酸反应生成氯化钡、水和二氧化碳;
(2)碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠;
氯化钡和硝酸银反应生成白色沉淀氯化银,盐酸和硝酸银反应生成白色沉淀氯化银和硝酸;
(3)降低温度能使氯化钡的浓溶液析出晶体;
(4)氯化钡能够溶于水,也能够溶于饱和氯化钠溶液,不能溶于饱和氯化钡溶液.
解答 解:(1)毒重石要进行粉碎的目的是:增大反应物的接触面积,加快反应的进行,气体X是BaCO3与稀盐酸反应生成的二氧化碳,所以X的化学式为CO2.
故填:增大反应物的接触面积,加快反应速率;CO2.
(2)检验滤渣是否洗净的试剂,实际上就是检验溶液中是不是还含有BaCl2,可以用碳酸钠溶液来检验,发生反应的化学方程式为:Na2CO3+BaCl2═BaCO3↓+2NaCl,试剂若是用硝酸银溶液,则发生的反应可能是:BaCl2+2AgNO3=2AgCl↓+Ba(NO3)2,所以可能生成的沉淀的化学式为AgCl,也可能是过量的盐酸与硝酸银溶液反应生成的AgCl,故此沉淀的直接来源可能有2个.
故填:BaCl2+Na2CO3═BaCO3↓+2NaCl;AgCl;2.
(3)经过操作Y,BaCl2溶液结晶析出BaCl2,故该操作应该是降温结晶,滤液2中可循环利用的物质除水外还有BaCl2.
故填:降温结晶;BaCl2.
(4)氯化钡能够溶于水,也能够溶于饱和氯化钠溶液,不能溶于饱和氯化钡溶液,因此洗涤氯化钡制品最适宜的洗涤剂是30℃饱和氯化钡溶液.
故填:C.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6.去年4月5日,科学家成功合成了第117号新元素,填补了第116号和118号元素之间的空缺.推测该元素为117号元素的依据是( )
| A. | 中子数 | B. | 质子数 | C. | 最外层电子数 | D. | 相对原子质量 |
4.对如图所示的实验说法正确的是( )
| A. | 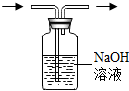 用该装置除去CO中的CO2的实验过程中无明显现象,因此不能达到实验目的 用该装置除去CO中的CO2的实验过程中无明显现象,因此不能达到实验目的 | |
| B. | 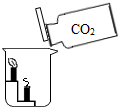 实验说明二氧化碳不燃烧也不支持燃烧,密度比空气大 实验说明二氧化碳不燃烧也不支持燃烧,密度比空气大 | |
| C. | 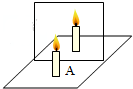 蜡烛A逐渐靠近玻璃板,蜡烛A的像逐渐变大 蜡烛A逐渐靠近玻璃板,蜡烛A的像逐渐变大 | |
| D. | 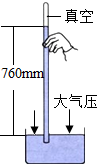 将玻璃管上移会使水银柱的高度增加 将玻璃管上移会使水银柱的高度增加 |
11.将H2、O2和N2的混合气体20g点燃,完全反应后生成18g水,下列情况中.不可能的是( )
| A. | 原混合气体中,H2的质量大于2g,同时氧气的质量小于16g | |
| B. | 原混合气体中,H2的质量大于2g,同时氧气的质量等于16g | |
| C. | 剩余的2g气体为N2 | |
| D. | 剩余的2g气体中含有H2、O2、N2 |
10.下列说法正确的是( )
| A. | 纯水是中性的,所以它的pH等于7 | |
| B. | 银跟盐酸起反应,生成氯化银和氢气 | |
| C. | 混有水蒸气的CO2通过NaOH固体后,得到干燥的CO2 | |
| D. | 凡能电离产生OH-离子的化合物叫做碱 |
14.下到事实和相应的解释一致的是( )
| A. | 真金不怕火炼一一说明金的熔点很高: | |
| B. | 干冰升华变为气体,所占体积变大--气体分子变大 | |
| C. | 金刚石用于钻探矿层--金刚石硬度大: | |
| D. | 燃烧的蜡烛被吹灭--可燃物与空气隔绝 |
15.下列图象不能正确反映其对应的实验操作的是( )
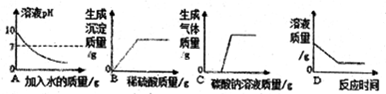

| A. | 常温下向pH=10的NaOH溶液不断加入水稀释 | |
| B. | 向一定量的氢氧化钠和氯化钡的混合溶液中滴加稀硫酸 | |
| C. | 向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| D. | 向一定质量的饱和石灰水中加过量的生石灰 |
 人类的生产生活离不开金属材料.
人类的生产生活离不开金属材料.