题目内容
9. 如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )
如图是a、b、c三种物质的溶解度曲线,下列分析不正确的是( )| A. | t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c | |
| B. | t2℃时,将30g a物质放入50g水中充分溶解得到a的饱和溶液75 g(a物质不含结晶水) | |
| C. | 将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,所得溶液溶质质量分数的关系是b>a=c | |
| D. | 将c的饱和溶液变为不饱和溶液,可采用降温的方法 |
分析 A、据固体的溶解度曲线可以:比较不同物质在同一温度下的溶解度大小;
B、据溶解度曲线可查出某物质在一定温度下的溶解度,从而判断饱和溶液的质量;
C、据物质的溶解度随温度变化情况及饱和溶液中溶质的质量分数分析解答;
D、c的溶解度随温度降低而增大,所以将其饱和溶液变为不饱和溶液可采取降温的方法.
解答 解:A、t2℃时,a、b、c三种物质的溶解度由大到小的顺序是a>b>c,正确;
B、t2℃时a的溶解度是50g,即100g水中最多溶解50g的a,所以将30g a物质放入50g水中充分溶解,剩余5g的a,得到a的饱和溶液75 g,正确;
C、将t2℃时a、b、c三种物质的饱和溶液降温至t1℃时,ab溶解度减小,析出晶体,溶质的质量分数减小,c溶解度变大,溶质质量分数与降温前相等,变为不饱和溶液;饱和溶液中溶质的质量分数=$\frac{溶解度}{溶解度+100g}$×100%,即溶解度大则溶质的质量分数大,而降温后b的溶解度大于a的溶解度大于降温前c的溶解度,故所得溶液溶质质量分数的关系是b>a>c,故错误;
D、c的溶解度随温度降低而增大,所以将其饱和溶液变为不饱和溶液可采取降温的方法,正确;
故选:C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
20.除去下列物质中少量杂质(括号内为杂质)的方法中,不能达到目的是( )
| A. | KNO3溶液(K2SO4)加入适量硝酸钡溶液后过滤 | |
| B. | Fe粉(Fe2O3)通入足量的一氧化碳气体加热后冷却 | |
| C. | CaO(CaCO3)将固体高温加热至质量恒定后冷却 | |
| D. | CO2气体(HCl)将气体通过澄清石灰水后干燥 |
17.化学就在我们身边,下列对化学的认识正确的是( )
| A. | 化石燃料的直接利用,促进了“低碳”经济的发展 | |
| B. | 档案室内资料着火,立即用水基型灭火器灭火 | |
| C. | 为了节约粮食,霉变大米虽然含有黄曲霉素,但蒸煮后可以用来喂猪 | |
| D. | 玻璃钢既不是玻璃也不是钢,而是复合材料 |
14.自来水是我国目前主要的生活饮用水,如表是我国颁布的生活饮用水水质标准的部分内容.
(1)感官指标表现的是自来水的物理性质(填“物理”或“化学”);
(2)自来水属于混合物(填“纯净物”或“混合物”); 除去水中不溶性杂质的操作方法是过滤.
(3)净化水的程度最高方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏
(4)长期饮用蒸馏水不利于(填“利于”或“不利于”)人体健康.
| 项目 | 标准 |
| 感官指标 | 无异味、异臭等 |
| 化学指标 | pH6.5-8.5,铜<1.0mg•L-1,铁<0.3mg•L-1,氟化物<1.0mg•L-1,游离氯≥0.3mg•L-1等 |
(2)自来水属于混合物(填“纯净物”或“混合物”); 除去水中不溶性杂质的操作方法是过滤.
(3)净化水的程度最高方法是D(填序号).
A.吸附 B.沉淀 C.过滤 D.蒸馏
(4)长期饮用蒸馏水不利于(填“利于”或“不利于”)人体健康.
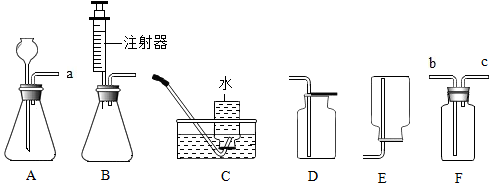
 现以锌和稀盐酸为原料制取和收集纯净、干燥的氢气.制取的氢气中常含有少量HCl气体和水分,可使用下列装置对气体进行净化.
现以锌和稀盐酸为原料制取和收集纯净、干燥的氢气.制取的氢气中常含有少量HCl气体和水分,可使用下列装置对气体进行净化.