题目内容
医学上经常用硫酸亚铁糖衣片给贫血患者补铁.某兴趣小组对这种糖衣片产生了兴趣,打算对药片的糖衣所起作用等问题进行探究.
【提出问题】硫酸亚铁糖衣片中糖衣的作用是什么?
【查阅资料】
(1)亚铁离子遇具有氧化性的物质易被氧化成铁离子;
(2)亚铁盐溶于水时,会与水电离产生的少量氢氧根离子生成Fe(OH)2沉淀.
(3)硫酸亚铁晶体加热会失去结晶水,高温会继续分解产生金属氧化物和非金属氧化物.
【提出猜想】药片糖衣的作用除了包装药物外,还可能是 .
【探究一】利用废水回收铜,制备硫酸亚铁晶体并观察其在空气中的变化推断糖衣的作用.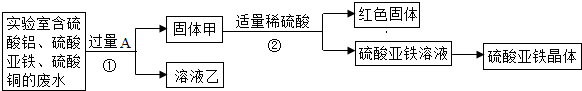
(1)固体甲中含有的物质是: 红色固体是 ;溶液乙中溶质是 .
(2)写出步骤①的化学方程式: ;检验步骤①向废液中加入A是否过量的方法是 ;实验中硫酸亚铁溶液中没有浑浊出现的原因可能是: .
【探究二】某硫酸亚铁晶体(FeSO4?xH2O)热分解研究
该兴趣小组同学称取ag硫酸亚铁晶体样品按如图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出X的值.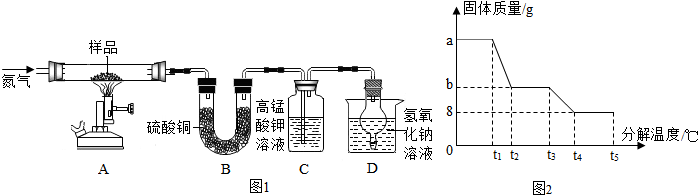
(3)①装置B中硫酸铜粉末变蓝,质量增咖12.6g,说明产物中有 ,装置C中高锰酸钾溶液褪色,说明产物中还有 .
②实验中要持续通入氮气,否则测出的X值会: (填“偏大”、“偏小”或“不变”),原因是: .
③硫酸亚铁晶体完全分解后装置A中固体呈红棕色,放入足量稀盐酸,固体全部溶解,得到黄色溶液,则装置A中红棕色固体是 .
④D装置中球形干燥管的作用是 ,氢氧化钠溶液的作用是 .
⑤小明从理论上分析得出硫酸亚铁晶体分解还生成另一种物质SO3,请你说出他这样判断的理论依据: .他打算向装置D中滴入紫色石蕊试液,小红认为此法不能达到实验的目的,小红这样判断的理由是: .
(4)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4?xH2O)进行热分解,获得相关数据,绘制成固体质量---分解温度的关系图如图2所示:
①图中t3至t4过程的化学反应方程式为: .
②计算FeSO4?xH2O中的X(写出计算过程)
【提出问题】硫酸亚铁糖衣片中糖衣的作用是什么?
【查阅资料】
(1)亚铁离子遇具有氧化性的物质易被氧化成铁离子;
(2)亚铁盐溶于水时,会与水电离产生的少量氢氧根离子生成Fe(OH)2沉淀.
(3)硫酸亚铁晶体加热会失去结晶水,高温会继续分解产生金属氧化物和非金属氧化物.
【提出猜想】药片糖衣的作用除了包装药物外,还可能是
【探究一】利用废水回收铜,制备硫酸亚铁晶体并观察其在空气中的变化推断糖衣的作用.

(1)固体甲中含有的物质是:
(2)写出步骤①的化学方程式:
【探究二】某硫酸亚铁晶体(FeSO4?xH2O)热分解研究
该兴趣小组同学称取ag硫酸亚铁晶体样品按如图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B的质量测出X的值.

(3)①装置B中硫酸铜粉末变蓝,质量增咖12.6g,说明产物中有
②实验中要持续通入氮气,否则测出的X值会:
③硫酸亚铁晶体完全分解后装置A中固体呈红棕色,放入足量稀盐酸,固体全部溶解,得到黄色溶液,则装置A中红棕色固体是
④D装置中球形干燥管的作用是
⑤小明从理论上分析得出硫酸亚铁晶体分解还生成另一种物质SO3,请你说出他这样判断的理论依据:
(4)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4?xH2O)进行热分解,获得相关数据,绘制成固体质量---分解温度的关系图如图2所示:
①图中t3至t4过程的化学反应方程式为:
②计算FeSO4?xH2O中的X(写出计算过程)
考点:实验探究物质的性质或变化规律,常见气体的检验与除杂方法,盐的化学性质,书写化学方程式、文字表达式、电离方程式,根据化学反应方程式的计算
专题:科学探究
分析:由题目的信息可知:药片糖衣的作用除了包装药物外,还可能是:隔绝空气,防止药品变质;在废液中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁,铁与硫酸铝不反应,因此甲中的固体是铁和铜,乙中的溶质有硫酸铝和硫酸亚铁;检验步骤①向废液中加入A是否过量的方法是:插入铁片,观察铁片表面是否出现红色物质:实验中硫酸亚铁溶液中没有浑浊出现的原因可能是:步骤②稀硫酸过量.装置B中硫酸铜粉末变蓝,质量增咖12.6g,说明产物中有水;装置C中高锰酸钾溶液褪色,说明产物中还有二氧化硫;实验中要持续通入氮气,否则测出的X值会:偏小;原因是:生成的部分水蒸气会在装置A处玻璃导管内冷凝;装置A中红棕色固体是氧化铁;D装置中球形干燥管的作用是:防止倒吸;氢氧化钠溶液的作用是:吸收SO2气体;小明从理论上分析得出硫酸亚铁晶体分解还生成另一种物质SO3,请你说出他这样判断的理论依据:每2个FeSO4分子分解生成1个Fe2O3后剩余S、O原子个数比为2:5不等于1:2;他打算向装置D中滴入紫色石蕊试液,小红认为此法不能达到实验的目的,小红这样判断的理由是:SO2溶于水能够生成亚硫酸;
解答:解:【提出猜想】药片糖衣的作用除了包装药物外,还可能是:隔绝空气,防止药品变质;故答案为:隔绝空气,防止药品变质
【探究一】在废液中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁,铁与硫酸铝不反应,因此甲中的固体是铁和铜,乙中的溶质有硫酸铝和硫酸亚铁;(1)故答案为:Fe、Cu; Cu;Al2(SO4)3 FeSO4
(2)铁与硫酸铜反应生成铜和硫酸亚铁,检验步骤①向废液中加入A是否过量的方法是:插入铁片,观察铁片表面是否出现红色物质:实验中硫酸亚铁溶液中没有浑浊出现的原因可能是:步骤②稀硫酸过量;故答案为:Fe+CuSO4=Cu+FeSO4 插入铁片,观察铁片表面是否出现红色物质 步骤②稀硫酸过量
【探究二】(3)装置B中硫酸铜粉末变蓝,质量增咖12.6g,说明产物中有水;装置C中高锰酸钾溶液褪色,说明产物中还有二氧化硫;实验中要持续通入氮气,否则测出的X值会:偏小;原因是:生成的部分水蒸气会在装置A处玻璃导管内冷凝;装置A中红棕色固体是氧化铁;D装置中球形干燥管的作用是:防止倒吸;氢氧化钠溶液的作用是:吸收SO2气体;小明从理论上分析得出硫酸亚铁晶体分解还生成另一种物质SO3,请你说出他这样判断的理论依据:每2个FeSO4分子分解生成1个Fe2O3后剩余S、O原子个数比为2:5不等于1:2;他打算向装置D中滴入紫色石蕊试液,小红认为此法不能达到实验的目的,小红这样判断的理由是:SO2溶于水能够生成亚硫酸;故答案为:①水 SO2 ②偏小 生成的部分水蒸气会在装置A处玻璃导管内冷凝 ③Fe2O3④防止倒吸 吸收SO2气体. ⑤每2个FeSO4分子分解生成1个Fe2O3后剩余S、O原子个数比为2:5不等于1:2 SO2溶于水能够生成亚硫酸
(4)硫酸亚铁在高温的条件下生成氧化铁和二氧化硫和三氧化硫,配平即可,故答案为:①2FeSO4
Fe2O3+SO2↑+SO3
②Fe2O3~2XH2O
160 36X
8g 12.6g
=
X=7
故答案为:7;
【探究一】在废液中加入过量的铁粉,铁与硫酸铜反应生成铜和硫酸亚铁,铁与硫酸铝不反应,因此甲中的固体是铁和铜,乙中的溶质有硫酸铝和硫酸亚铁;(1)故答案为:Fe、Cu; Cu;Al2(SO4)3 FeSO4
(2)铁与硫酸铜反应生成铜和硫酸亚铁,检验步骤①向废液中加入A是否过量的方法是:插入铁片,观察铁片表面是否出现红色物质:实验中硫酸亚铁溶液中没有浑浊出现的原因可能是:步骤②稀硫酸过量;故答案为:Fe+CuSO4=Cu+FeSO4 插入铁片,观察铁片表面是否出现红色物质 步骤②稀硫酸过量
【探究二】(3)装置B中硫酸铜粉末变蓝,质量增咖12.6g,说明产物中有水;装置C中高锰酸钾溶液褪色,说明产物中还有二氧化硫;实验中要持续通入氮气,否则测出的X值会:偏小;原因是:生成的部分水蒸气会在装置A处玻璃导管内冷凝;装置A中红棕色固体是氧化铁;D装置中球形干燥管的作用是:防止倒吸;氢氧化钠溶液的作用是:吸收SO2气体;小明从理论上分析得出硫酸亚铁晶体分解还生成另一种物质SO3,请你说出他这样判断的理论依据:每2个FeSO4分子分解生成1个Fe2O3后剩余S、O原子个数比为2:5不等于1:2;他打算向装置D中滴入紫色石蕊试液,小红认为此法不能达到实验的目的,小红这样判断的理由是:SO2溶于水能够生成亚硫酸;故答案为:①水 SO2 ②偏小 生成的部分水蒸气会在装置A处玻璃导管内冷凝 ③Fe2O3④防止倒吸 吸收SO2气体. ⑤每2个FeSO4分子分解生成1个Fe2O3后剩余S、O原子个数比为2:5不等于1:2 SO2溶于水能够生成亚硫酸
(4)硫酸亚铁在高温的条件下生成氧化铁和二氧化硫和三氧化硫,配平即可,故答案为:①2FeSO4
| ||
②Fe2O3~2XH2O
160 36X
8g 12.6g
| 160 |
| 36X |
| 8g |
| 12.6g |
故答案为:7;
点评:本考点既考查了实验步骤的设计,又考查了化学方程式的书写和有关的计算,还对实验进行了评价,综合性比较强.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质长时间敞口放置在空气中,质量会增加且有新物质生成的是( )
| A、硫酸钡 | B、浓硫酸 |
| C、浓盐酸 | D、苛性钠 |
下列变化属于化学变化的是( )
| A、自行车内胎爆炸 |
| B、汽油挥发 |
| C、水结成冰 |
| D、水通电产生氢气和氧气 |
厨房里发生的下列变化中,属于物理变化的是( )
| A、苹果腐烂 | B、黄瓜榨汁 |
| C、面包发霉 | D、菜刀锈蚀 |
 如果把物质按单质、氧化物、酸、碱、盐、有机物分类,图中甲、乙、丙是三种不同类别的物,且相连物质间均能发生化学反应,下列说法不正确的是( )
如果把物质按单质、氧化物、酸、碱、盐、有机物分类,图中甲、乙、丙是三种不同类别的物,且相连物质间均能发生化学反应,下列说法不正确的是( )| A、当甲为氯化铵时,X可以为氢氧化钾 |
| B、当甲、乙、丙为酸碱盐时,X可以为碳酸钠 |
| C、当X为氧气时,甲、乙、丙可以为单质、氧化物、有机物 |
| D、当X为稀硫酸时,甲、乙、丙可以为氢氧氧钡、氯化钡和氢氧化钠 |
2011年,中国西南5省市区遭受历史罕见的大旱.云南,广西部分地区的旱情已达到特大干旱的程度,贵州省秋冬连旱,出现80年一遇,部分地区的旱情甚至百年一遇.这一灾难再次向我们敲响警钟:水是生命之源,我们要珍惜水、保护水.下列行为应积极提倡的是( )
| A、生活污水任意排放 |
| B、洗完衣服的水用来冲厕所 |
| C、做完酸碱中和实验后,将废液倒入下水道 |
| D、禁止使用地下水 |
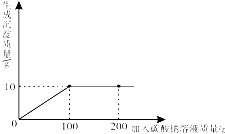 小亮同学在某化工厂进行社会实践,技术员与小亮一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量.现取14.4g固体样品,全部溶于95.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.试求:(本题计算结果保留一位小数)
小亮同学在某化工厂进行社会实践,技术员与小亮一起分析由氯化钙和氯化钠组成的产品中氯化钠的含量.现取14.4g固体样品,全部溶于95.6g水中,向所得的混合溶液中滴加溶质质量分数为10.6%的碳酸钠溶液,记录了如图所示的曲线关系.试求:(本题计算结果保留一位小数)