题目内容
11.某金属的氯化物溶液200g,溶质质量分数为5.55%.向其中滴加AgNO3溶液至不再产生沉淀为止,过滤、干燥得固体28.7g.该金属氯化物的化学式应为( )| A. | NaCl | B. | MgCl2 | C. | FeCl3 | D. | CaCl2 |
分析 根据氯化物与硝酸银通过交换成分可生成氯化银及反应前后元素质量不变,由反应生成氯化银中氯元素质量及该氯化物的质量,计算氯化物中两元素的质量比,根据组成元素质量比确定选项中所提供的化学为该金属氯化物的化学式;其中需要使用溶液的质量与溶液的质量分数计算氯化物的质量.
解答 解:该金属氯化物的质量=200g×5.55%=11.1g;
该金属氯化物中氯元素的质量=28.7g×$\frac{35.5}{143.5}×$100%=7.1g
该金属氯化物中金属元素与氯元素的质量比=(11.1g-7.1g):7.1g=40:71.
A、NaCl中金属元素钠与氯元素的质量比=23:35.5=46:71,故A错误;
B、MgCl2中金属元素镁与氯元素的质量比=24:(35.5×2)=24:71,故B错误;
C、FeCl3中金属元素铁与氯元素的质量比=56:(35.5×3)=112:213,故C错误.
D、CaCl2中金属元素钙与氯元素的质量比=40:(35.5×2)=40:71,故D正确;
故选D.
点评 根据物质的化学式,组成元素的质量比等于各元素的相对原子质量与原子个数乘积的比.

练习册系列答案
相关题目
6.下列东台特产中,维生素含量最高的是( )
| A. | 弶港海鲜 | B. | 富安鱼汤面 | C. | 三仓西瓜 | D. | 溱东青浦螃蟹 |
3.化学是以实验为基础的自然科学,下列实验操作正确的是( )
| A. |  给液体加热 | B. | 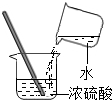 稀释浓硫酸 | C. |  气体验满 | D. |  倾倒液体 |
20.钙元素对人类生命和生活具有重要意义,含钙的物质是中学化学研究的重要内容.

(1)如图为元素周期表中钙元素的相关信息及钙原子结构示意图,下列说法不正确的是C(填标号).
A.钙原子核内有20个质子 B.钙的相对原子质量40.08
C.钙元素位于第二周期性 D.钙原子在化学反应中容易失去电子
(2)钙是人体内含量最高的金属元素,儿童缺钙易患佝偻病;钙在人体中主要以羟基磷酸钙【Cax(PO4)6(OH)2]的形式存在,已知该化合物中磷的化合价为+5,则x应为10.
(3)某化学兴趣小组的同学对一瓶颈久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动.
【提出问题】这瓶熟石灰粉末的变质程度.
【进行猜想】猜想一:熟石灰全部变成了CaCO3;
猜想二:熟石灰部分变成了CaCO3;
猜想三:熟石灰没有变质.
【设计实验】该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容.
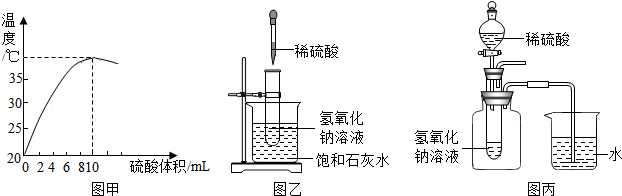
(4)如图是某趣味实验装置图,其气密性良好,打工分液漏斗,使其中的无色液体与烧瓶中的固体接触反应,可观察到B中尖嘴导管口有“喷泉”产生.请分别写出一个符合上述现象和下列要求的化学方程式.
①化合反应CaO+H2O=Ca(OH)2;
②复分解反应Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(5)为解决鱼池中氧气不足的问题,可用固体过氧化钙(CaO)作增氧剂,过氧化钙与水反应生成氢氧化钙和氧气,7.2g过氧化钙与足量的水反应,生成氧气的质量是多少?

(1)如图为元素周期表中钙元素的相关信息及钙原子结构示意图,下列说法不正确的是C(填标号).
A.钙原子核内有20个质子 B.钙的相对原子质量40.08
C.钙元素位于第二周期性 D.钙原子在化学反应中容易失去电子
(2)钙是人体内含量最高的金属元素,儿童缺钙易患佝偻病;钙在人体中主要以羟基磷酸钙【Cax(PO4)6(OH)2]的形式存在,已知该化合物中磷的化合价为+5,则x应为10.
(3)某化学兴趣小组的同学对一瓶颈久置的熟石灰粉末的组成进行实验探究,请你一起参与他们的探究活动.
【提出问题】这瓶熟石灰粉末的变质程度.
【进行猜想】猜想一:熟石灰全部变成了CaCO3;
猜想二:熟石灰部分变成了CaCO3;
猜想三:熟石灰没有变质.
【设计实验】该小组同学对猜想一设计了下列探究方案,请你帮助他们完成下表中相关实验内容.
| 实验步骤 | 实验现象 | 实验结论 |
| ①取样,加适量水,搅拌,过滤 ②取少量滤液于试管中,滴入酚酞溶液 ③取少量滤渣于试管中,加入盐酸 | ②试液没有变成红色 ③滤渣溶解,产生气泡 | 猜想一成立 |
①化合反应CaO+H2O=Ca(OH)2;
②复分解反应Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(5)为解决鱼池中氧气不足的问题,可用固体过氧化钙(CaO)作增氧剂,过氧化钙与水反应生成氢氧化钙和氧气,7.2g过氧化钙与足量的水反应,生成氧气的质量是多少?
 水和溶液在生命活动、生产和生活中有着重要的作用.请回答下列与水和溶液有关的问题:
水和溶液在生命活动、生产和生活中有着重要的作用.请回答下列与水和溶液有关的问题: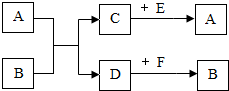 A、B、C、D、E、F都是初中化学中常见的物质,A、C组成元素相同,DWie红色固体单质,它们之间的相互转化如下:(图中“→”表示物质间存在的转化关系,反应条件已略去)
A、B、C、D、E、F都是初中化学中常见的物质,A、C组成元素相同,DWie红色固体单质,它们之间的相互转化如下:(图中“→”表示物质间存在的转化关系,反应条件已略去)