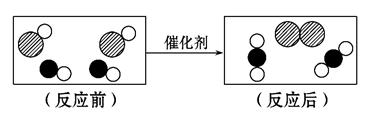
题目内容
工业上用“侯氏制碱法”生产的纯碱(Na2CO3)中往往含有少量的氯化钠。现将12g含有氯化钠的纯碱加入到一定量的溶质的质量分数为14.6%稀盐酸中,恰好完全反应,收集到4.4g的气体(假设生成的气体全部逸出)。
已知:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
计算反应后得到氯化钠溶液的质量。
【解】设:稀盐酸中溶质HCl的质量为x。
Na2CO3 + 2HCl === 2NaCl + H2O + CO2↑
73 44
x 4.4g
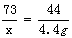
x = 7.3g ……………………1分
稀盐酸的质量= 7.3g / 14.6% = 50g ……………………1分
反应后得到氯化钠溶液的质量= 12g + 50g - 4.4g = 57.6g ……………………1分
答:反应后得到氯化钠溶液的质量为57.6g。(其它合理解法均可)

练习册系列答案
 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案 小题狂做系列答案
小题狂做系列答案
相关题目
某水泥厂化验室,为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水.)有关实验数据如下表:
| 反应前 | 反应后 | ||
| 实 验 数 据 | 烧杯和稀盐酸 的质量 | 石灰石样品 的质量 | 烧杯和其中混 合物的质量 |
| 150g | 12g | 157.6g |
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为 g.
(2)求该石灰石中碳酸钙的质量分数.
 (2)B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是 (用化学式表示),D物质的一种用途是 。
(2)B溶液在一定条件下可反应生成C和无色气体D,C和D都与生命活动息息相关。B溶液中的溶质是 (用化学式表示),D物质的一种用途是 。