题目内容
7.如图是实验室抽取和收集气体的常用装置,请回答问题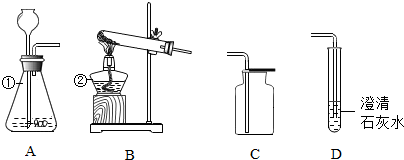
(1)指出图中标号的仪器名称:
①长颈漏斗,②酒精灯.
(2)实验室抽取气体时均应先检查装置的气密性,请描述如何检查B装置的气密性?
(3)由于CO2具有不燃烧、不支持燃烧,密度比空气的大的性质,日常生活中常用它来灭火.
(4)将装置A(制取CO2)与D相连接,观察到的现象是清的石灰水变浑浊,对该变化的解释(用化学方程式回答)CO2+Ca(OH)2=CaCO3↓+H2O.
(5)小明为了测定贝壳中碳酸钙的含量,他将贝壳粉碎后取样品10g与足量的稀盐酸充分反应(杂质不与盐酸反应),结果发现,反应后的总质量比反应前的总质量减少了1.76g,计算贝壳中碳酸钙的质量?
分析 (1)根据实验室常用仪器解答;
(2)根据检验装置气密性的方法解答;
(3)根据二氧化碳的密度比空气的大,不支持燃烧解答;
(4)检验二氧化碳通常用澄清的石灰水;
(5)根据质量守恒定律,减少的质量为生成的二氧化碳的质量;利用二氧化碳的质量可以计算反应碳酸钙的质量.
解答 解:
(1)根据实验室常用仪器可知:①长颈漏斗;②酒精灯;
(2)检查装置的气密性气密性的方法是先把导管放入水中,然后两只手紧握试管,导管口有气泡产生说明气密性良好;
(3)二氧化碳的密度比空气的大,不燃烧、不支持燃烧,日常生活中常用它来灭火;
(4)通常用澄清的石灰水来检验二氧化碳的存在,因为二氧化碳能使澄清的石灰水变浑浊,也就是生成了不溶于水的碳酸钙;故填:澄清的石灰水变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O;
(5)根据质量守恒定律,减少的质量为生成的二氧化碳的质量,
设碳酸钙的质量为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 44
x 1.76g
$\frac{100}{x}=\frac{44}{1.76g}$
x=4g
答案:
(1)①长颈漏斗;②酒精灯;
(2)先把导管放入水中,然后两只手紧握试管,导管口有气泡产生说明气密性良好;
(3)不燃烧、不支持燃烧,密度比空气的大;
(4)清的石灰水变浑浊;CO2+Ca(OH)2=CaCO3↓+H2O;
(5)贝壳中碳酸钙的质量为4g.
点评 本题是考查与二氧化碳的实验室制法和性质有关的一系列知识要点(比如实验装置、化学方程式、验证方法),所以要求学生对二氧化碳的实验制法要加以延伸理解.

练习册系列答案
相关题目
15.下列化学式书写正确的是( )
| A. | 氧化钙CaO | B. | 氧化铝Al2O3 | C. | 氢氧化钠Na(OH)2 | D. | 氧化镁OMg |
2. 将相同状态的铁和镁分别与相同质量分数,足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是( )
将相同状态的铁和镁分别与相同质量分数,足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是( )
 将相同状态的铁和镁分别与相同质量分数,足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是( )
将相同状态的铁和镁分别与相同质量分数,足量的稀盐酸反应,产生氢气的质量与反应时间的关系如图所示,下列说法正确的是( )| A. | 铁和镁的质量相同 | |
| B. | 甲是铁、乙是镁 | |
| C. | 反应后溶液的质量均减少 | |
| D. | 铁和镁完全反应所消耗的稀盐酸质量相同 |
12.雾霾天气给人们的生产、生活和健康带来了影响,保护环境、合理开发与利用能源已受到人们的普遍关注.下列说法错误的是( )
| A. | 减少化石燃料的使用,多开发利用太阳能、风能、地热能等 | |
| B. | 减少使用私家车次数,多乘公交车或骑自行车,实现“低碳生活” | |
| C. | 尽量多使用一次性餐具,既方便又卫生 | |
| D. | 废旧电池不随意丢弃,可回收利用以便节约金属资源并减少污染 |
19.除去下列物质中的少量杂质,不正确的是( )
| 选项 | 物质 | 杂质 | 试剂或方法 |
| A | CaCl2溶液 | HCl | 过量的CaCO3过滤 |
| B | NaOH溶液 | Ca(OH)2 | 过量的Na2CO3溶液,过滤 |
| C | N2 | O2 | 通过灼热的铜网 |
| D | H2 | 水蒸气 | 通过盛有浓硫酸的洗气瓶 |
| A. | A | B. | B | C. | C | D. | D |

