题目内容
在天平两托盘上各放置一只烧杯,在两只烧杯中注入等质量、等质量分数的稀盐酸,然后在左边的烧杯中放入金属镁,在右边的烧杯中放入等质量的金属铝.待充分反应后,可判断:(1)若天平保持平衡,反应物 一定剩余, 一定没有剩余, 可能剩余.
(2)若天平失去平衡,一定是 边(填“左”或“右”)的托盘往下沉.
【答案】分析:根据金属与酸反应的化学方程式进行计算,可以从金属足量以及酸足量的角度进行分析完成.
(1)天平保持平衡,说明生成气体一样多,稀盐酸一定没有剩余;再根据化学方程式计算判断铝、镁是否有剩余;
(2)若天平失去平衡,说明稀盐酸有剩余,根据计算结果判断镁铝的剩余.
解答:解:假设铝和镁的质量为1g,则可以根据化学方程式来求算出它们所产生的气体的质量,然后进行比较;
设1g铝所产生的气体的质量为X
2Al+6HCl═2AlCl3+3H2↑
54 6
1g X
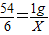
解得:X=0.11g
设1g镁可以所产生的气体的质量为y
Mg+2HCl═MgCl2+H2↑
24 2
1g y
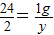
解得:y=0.08g
(1)根据题意可以知道若天平平衡,则生成气体的质量相等,所以根据刚才的计算可以得出铝有剩余,而稀盐酸完全反应;
(2)根据题意可以知道等质量的铝和镁与足量的稀盐酸反应时生成铝生成的气体较多,即放金属铝的那一边质量减少的多,即右盘轻而左盘重,所以天平将会向左盘倾斜;
故答案为:(1)铝(或Al);稀盐酸;镁(或Mg);
(2)左.
点评:本题主要考查学生灵活运用化学方程式进行计算的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.
(1)天平保持平衡,说明生成气体一样多,稀盐酸一定没有剩余;再根据化学方程式计算判断铝、镁是否有剩余;
(2)若天平失去平衡,说明稀盐酸有剩余,根据计算结果判断镁铝的剩余.
解答:解:假设铝和镁的质量为1g,则可以根据化学方程式来求算出它们所产生的气体的质量,然后进行比较;
设1g铝所产生的气体的质量为X
2Al+6HCl═2AlCl3+3H2↑
54 6
1g X
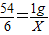
解得:X=0.11g
设1g镁可以所产生的气体的质量为y
Mg+2HCl═MgCl2+H2↑
24 2
1g y
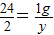
解得:y=0.08g
(1)根据题意可以知道若天平平衡,则生成气体的质量相等,所以根据刚才的计算可以得出铝有剩余,而稀盐酸完全反应;
(2)根据题意可以知道等质量的铝和镁与足量的稀盐酸反应时生成铝生成的气体较多,即放金属铝的那一边质量减少的多,即右盘轻而左盘重,所以天平将会向左盘倾斜;
故答案为:(1)铝(或Al);稀盐酸;镁(或Mg);
(2)左.
点评:本题主要考查学生灵活运用化学方程式进行计算的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目