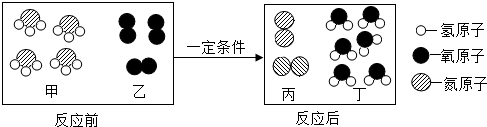
题目内容
8.向153.7g碳酸钠溶液中逐滴加入l00g溶质质量分数为20.8%的氯化钡溶液,恰好完全反应,所得溶液为不饱和溶液,请根据题意回答下列问题:(1)l00g溶质质量分数为20.8%的氯化钡溶液中氯化钡的质量为20.8g;
(2)生成沉淀的质量为19.7g;
(3)完全反应后所得溶液中溶质的质量分数为多少?
分析 (1)根据溶质质量=溶液质量和溶质质量分数的乘积进行分析;
(2)根据化学方程式和氯化钡的质量计算生成的碳酸钡的质量;
(3)根据化学方程式计算反应后生成的氯化钠,计算溶液的质量,然后计算溶质的质量分数.
解答 解:(1)l00g溶质质量分数为20.8%的氯化钡溶液中氯化钡的质量为100g×20.8%=20.8g;
(2)设生成碳酸钡沉淀质量为x,生成氯化钠的质量为y
Na2CO3 +BaCl2=BaCO3↓+2NaCl
208 197 117
20.8g x y
$\frac{208}{20.8g}$=$\frac{197}{x}$=$\frac{117}{y}$
x=19.7g
y=11.7g
(3)完全反应后所得溶液中溶质的质量分数为:$\frac{11.7g}{153.7g+100g-19.7g}$×100%=5%.
故答案为:(1)20.8;
(2)19.7;
(3)完全反应后所得溶液中溶质的质量分数为5%.
点评 本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
18.下列说法正确的是( )
| A. | 家里的铁质炊具使用后应该涂一点润滑油,以防止生锈 | |
| B. | 所有人类所利用的金属,其来源都是将金属从其化合物中通过化学反应变成单质 | |
| C. | 铝比铁活泼,所以家用的铝制器皿的腐蚀就会比铁制器皿要快一些 | |
| D. | 从铜器、铁器和铝制器皿的使用时期来看,人类利用金属单质的前后顺序还与其金属活动性顺序有关 |
19.下列关于“一定”的说法错误的是( )
| A. | 复分解反应的生成物一定都是化合物 | |
| B. | 无机物都是不含碳元素的化合物 | |
| C. | 所有的碱一定含有氢元素和氧元素 | |
| D. | 中和反应一定有水生成 |
16.实验操作考试结束后,某同学对仪器的处理方式正确的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
3.分析推理是化学学习常用的方法,下列分析推理正确的是( )
| A. | 浓盐酸具有挥发性,所以浓硫酸也具有挥发性 | |
| B. | 点燃羽毛闻到焦羽毛味,所以点燃头发也能闻到焦羽毛味 | |
| C. | 离子是带电荷的粒子,所以带电荷的粒子一定是离子 | |
| D. | 某有机物燃烧生成C02和H20,该有机物中一定含有C、H、0三种元素 |
13.实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣.
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中.
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分.
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③碳和氧化铜的混合物.
【设计方案】请帮助该同学完成下述实验报告:
探究二:碱式碳酸铜受热分解还会生成CO2和H2O.
【进行实验】选择如下图所示装置进行验证
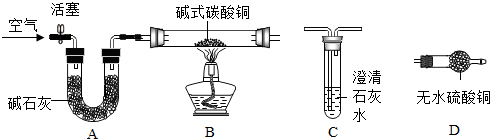
步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置A→B→D→C(填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热
【解释与结论】
①当观察到C中石灰水变浑浊,D中无水硫酸铜变蓝,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O;
②写出Cu2(OH)2CO3受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
【反思与评价】
上述装置中A的作用是除去空气中的水分和二氧化碳,防止对产物的检验造成干扰.
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中.
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分.
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③碳和氧化铜的混合物.
【设计方案】请帮助该同学完成下述实验报告:
| 实验操作与现象 | 实验结论 |
| 取黑色粉末,加入足量稀硫酸,充分反应后,黑色固体全部溶解形成蓝色溶液 | 猜想②正确 |
【进行实验】选择如下图所示装置进行验证

步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置A→B→D→C(填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热
【解释与结论】
①当观察到C中石灰水变浑浊,D中无水硫酸铜变蓝,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O;
②写出Cu2(OH)2CO3受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
【反思与评价】
上述装置中A的作用是除去空气中的水分和二氧化碳,防止对产物的检验造成干扰.
20.化学和我们的生活息息相关,下列知识归纳完全正确的一组是( )
| A.认识物质俗名 | B.注意实验安全 |
| ①冰一固体二氧化碳 ②熟石灰--氧化钙 | ①鉴别化学药品时可以品尝 ②可以直接去闻浓盐酸的气味 |
| C.合理利用资源 | D.健康生活方式 |
| ①合理使用农药、化肥提高农业产量 ②用人畜粪便、作物秸秆制取沼气 | ①药补不如食补,要均衡膳食 ②少量吸烟,可以使精神提高 |
| A. | A | B. | B | C. | C | D. | D |
17.南充盛产水果,素有“果城”的美誉,常见的水果中一般不含下列哪种营养素( )
| A. | 油脂 | B. | 维生素 | C. | 糖类 | D. | 水 |