题目内容
某生铁样品6克,投入到98克10%稀硫酸中恰好完全反应(样品杂质不与硫酸反应),计算该样品中杂质的质量分数是多少?( Fe:56 H:1 S:32 O:16 )
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据硫酸的质量可以求出样品中铁的质量,进而求得样品中杂质的质量分数.
解答:解:设该生铁样品中铁的质量为x
Fe十H2SO4=FeSO4+H2↑
56 98
x 98g×10%
=
x=5.6g
样品中杂质的质量分数:
×00%≈6.7%
答:样品中杂质的质量分数为6.7%.
Fe十H2SO4=FeSO4+H2↑
56 98
x 98g×10%
| 56 |
| 98 |
| x |
| 98g×10% |
x=5.6g
样品中杂质的质量分数:
| 6g-5.6g |
| 6g |
答:样品中杂质的质量分数为6.7%.
点评:反应的化学方程式可表示反应中各物质的质量关系,由反应中某物质的质量可计算该反应中其它物质的质量.

练习册系列答案
相关题目
在实验室中取用一定量的下列药品,可以用量筒的是( )
| A、盐酸 | B、锌粒 |
| C、食盐 | D、碳酸钠粉末 |
成语是中华民族的瑰宝.“釜底抽薪”中蕴含的灭火原理是( )
| A、隔绝空气 |
| B、移除可燃物 |
| C、降低温度到着火点以下 |
| D、提高可燃物的着火点 |
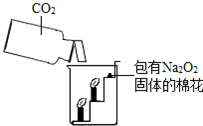 过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,同学们将包有Na2O2固体的棉花放入了如图所示的装置中,发现高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭,同时也惊奇地发现棉花燃烧了起来.
过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,同学们将包有Na2O2固体的棉花放入了如图所示的装置中,发现高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭,同时也惊奇地发现棉花燃烧了起来. 用五个圆表示:氧化铁、稀硫酸、碳酸钠、稀盐酸、氯化钡五种物质,相切的两圆可以发生反应,如图所示,在三个圆中填上适当的物质A
用五个圆表示:氧化铁、稀硫酸、碳酸钠、稀盐酸、氯化钡五种物质,相切的两圆可以发生反应,如图所示,在三个圆中填上适当的物质A