题目内容
7.下列排列顺序不正确的是( )| A. | 相对分子质量:二氧化碳>氮气>氢气 | |
| B. | 硫元素的化合价:Na2SO4>H2S>S | |
| C. | 空气中组成物质的含量:氮气>氧气>二氧化碳 | |
| D. | 地壳中元素含量:Fe<Al<Si |
分析 A.根据相对分子的质量为组成分子的各原子的相对原子质量之和,分别计算相对分子的质量进行比较;
B.根据在化合物中正负化合价代数和为零,分别计算硫元素的化合价进行比较,解答;
C.回顾空气的组成成分,判断所涉气体含量大小关系;
D.回顾地壳中各元素含量,判断所涉三种元素的含量大小关系.
解答 解:A.根据相对分子的质量为组成分子的各原子的相对原子质量之和,可得二氧化碳的相对分子质量为:12×2+16×2=44;氢气的相对分子质量为2;氮气的相对分子质量为14×2=28;故正确;
B.根据在化合物中正负化合价代数和为零,可得SO2中硫元素的化合价为 x+(-2)×2=0,x=+4;
Na2SO4中硫元素的化合价为 (+1)×2+y+(-2)×4=0,y=+6;
H2S中硫元素的化合价为 (+1)×2+z=0,z=-2;硫元素的化合价:Na2SO4>SO2>H2S;故错误;
C.空气的组成中,氮气占78%、氧气占21%、二氧化碳占0.03%,空气中组成物质的含量由大到小的是:氮气>氧气>二氧化碳;故正确;
D.地壳中元素含量前四位的元素依次为O、Si、Al、Fe,地壳中元素含量Fe<Al<Si的顺序是不正确的;故正确.
故选B.
点评 本题考查学生对相对分子的质量,化合价的计算,空气的组成,地壳里各元素的含量知识的理解与掌握,并能在解题中灵活应用的能力.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
17.某同学欲量取10毫升某液体,他将量筒放平稳,俯视量筒的刻度,则该同学量取实际液体量为( )10毫升.
| A. | 小于 | B. | 大于 | C. | 等于 | D. | 无法确定 |
12.由碳、氧两种元素组成的气体,碳与氧的质量之比为1:4,则该气体可能是( )
| A. | 由CO或CO2单独组成的纯净物 | B. | 由CO和CO2共同组成的混合物 | ||
| C. | 由CO和O2等质量组成的混合物 | D. | 由CO2和O2共同组成的混合物 |
19.下列关于氧气的说法中,不正确的是( )
| A. | 物质与氧气发生的反应都是氧化反应 | |
| B. | 将带火星的木条插入集气瓶中,木条不复燃,不一定没有氧气 | |
| C. | 鱼、虾等能在水中生存,是由于氧气不易溶于水 | |
| D. | 细铁丝在空气剧烈燃烧,剧烈燃烧,火星四射 |
1. 空气中氧气含量测定的再认识.
空气中氧气含量测定的再认识.
【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式.4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
【交流表达】
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据如表数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确..
 空气中氧气含量测定的再认识.
空气中氧气含量测定的再认识.【实验回顾】图1是实验室用红磷燃烧来粗略测定空气中氧气含量的装置.
(1)写出红磷燃烧的化学方程式.4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5
(2)实验原理:由于红磷燃烧消耗空气中的氧气,使瓶内气压减小,烧杯中水倒吸到集气瓶.若装置的气密性良好,操作规范,用量筒测量进入瓶中水的体积,能粗略测得空气中氧气的含量.
【问题提出】有实验资料表明:燃烧过程中当氧气体积分数低于7% 时,红磷就无法继续燃烧,因此通过上述实验,测置结果与理论值误差较大.
【实验改进】
Ⅰ.根据铁在空气中生锈的原理设计图2实验装置,再次测定空气中氧气含量.装置中饱和食盐水、活性炭会加速铁生锈.
Ⅱ.测得实验数据如表
| 测量项目 | 实验前 | 实验后 | |
| 烧杯中水的体积 | 烧杯中剩余水的体积 | 集气瓶(扣除内容物)和导管的容积 | |
| 体积/mL | 80.0 | 54.5 | 126.0 |
(1)铁生锈过程发生复杂的化学反应,首先是铁与氧气、水反应生成氢氧化亚铁[Fe(OH)2],写出该反应的化学方程式2Fe+2H2O+O2=2Fe(OH)2.
(2)根据如表数据计算,改进实验后测得的空气中氧气的体积分数是20.2%(计算结果精确到0.1%).
(3)从实验原理角度分析,改进后的实验结果比前者准确度更髙的原因是:①铁的缓慢氧化使集气瓶中的氧气消耗更彻底,使实验结果更准确;②测量时考虑到导管容积和扣除内容物后的集气瓶容积,使实验结果更准确..

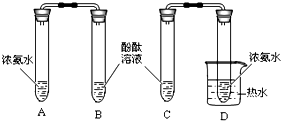 小明通过以下实验探究分子的某些性质,实验装置如下:
小明通过以下实验探究分子的某些性质,实验装置如下: