题目内容
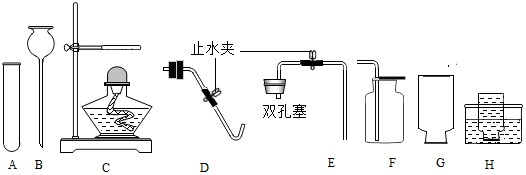
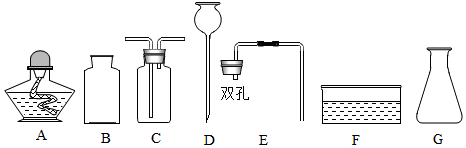
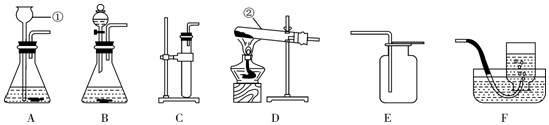
12.请用下列实验装置完成气体的制取及性质实验.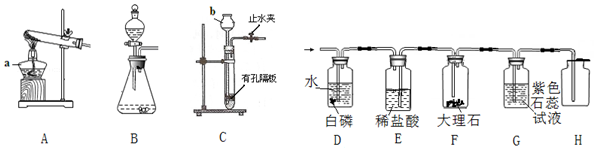
(1)写出仪器名称:a酒精灯,b长颈漏斗.
(2)用双氧水和二氧化锰混合制氧气,为了得到平稳的氧气流,应该选择的发生装置是B(填序号),反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;当产生的氧气从D的左边导管通入时,很快看到G中导管口有气泡冒出.D中白磷始终没有燃烧的原因是温度没有达到白磷的着火点;G中溶液由紫色变红色,G中颜色变化的原因是CO2+H2O=H2CO3(用化学方程式表示).
(3)实验过程中,E中观察到的现象是稀盐酸液面下降,有溶液流入F装置;F中反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(4)用H装置可以收集剩余气体,H装置收集气体的依据是气体的密度大于空气的密度.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用双氧水和二氧化锰制取氧气的反应物是固体和液体,反应条件是常温,分液漏斗可以控制液体的滴加速度,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,可燃物燃烧的条件,二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色进行分析;
(3)根据实验过程中,随着气体的通入,E中的气压逐渐增大,观察到的现象是:稀盐酸液面下降,有溶液流入F装置,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析;
(4)根据H装置收集气体的方法是:向上排空气法进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,a是酒精灯,b是长颈漏斗;
(2)实验室用双氧水和二氧化锰制取氧气的反应物是固体和液体,反应条件是常温,分液漏斗可以控制液体的滴加速度,所以为了得到平稳的氧气流,应该选择的发生装置是B,过氧化氢在二氧化锰的催化作用下分解生成水和氧气,化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,D中白磷始终没有燃烧的原因是:温度没有达到白磷的着火点,二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊变红色,化学方程式为:CO2+H2O=H2CO3;
(3)实验过程中,随着气体的通入,E中的气压逐渐增大,观察到的现象是:稀盐酸液面下降,有溶液流入F装置,碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)H装置收集气体的方法是:向上排空气法,所以H装置收集气体的依据是:气体的密度大于空气的密度.
故答案为:(1)酒精灯,长颈漏斗;
(2)B,2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,温度没有达到白磷的着火点,CO2+H2O=H2CO3;
(3)稀盐酸液面下降,有溶液流入F装置,CaCO3+2HCl=CaCl2+H2O+CO2↑;
(4)气体的密度大于空气的密度.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

 名校课堂系列答案
名校课堂系列答案| A. | 用食盐水消毒杀菌 | B. | 用霉变花生榨花生油 | ||
| C. | 用甲醛溶液保存海鲜 | D. | 用含亚硝酸钠的工业用盐烹调食物 |
| A. | 家庭自制冰块 | B. | 牛奶变酸 | C. | 糯米酿酒 | D. | 木柴燃烧 |