题目内容
3.某化学小组探究用大理石和稀盐酸反应制取二氧化碳气体,并进行性质实验.如图是有关实验的部分装置,请根据要求回答问题:
(1)a仪器的名称为长颈漏斗;甲同学用A和C组合制取二氧化碳,乙同学用B和C组合制取二氧化碳,你认为乙组合更便于控制反应发生与停止(填写甲或乙).
(2)某同学利用装置D进行性质实验时,观察到紫色石蕊试液变红色,将红色液体充分加热未能重新变为紫色,你认为可能的原因是H2O+CO2=H2CO3.
(3)能否利用装置C收集氢气,你的答案是不能,理由是氢气密度比空气的密度小.
分析 (1)由仪器的图和用途可知a为长颈漏斗;在A装置和B装置的特点去分析;
(2)从二氧化碳和紫色石蕊试液中的水反应生成碳酸,碳酸是一种酸,可以使紫色石蕊溶液变红色去分析;
(3)氢气难溶于水,密度比空气的密度小,因此可以用排水法和向下排空气法收集.
解答 解:(1)由仪器的图和用途可知a为长颈漏斗;在A装置中一旦石灰石和稀盐酸反应,则只有在至少一种反应物反应完全后,反应才能停止;而在B装置中,把石灰石放在隔板上,稀盐酸通过长颈漏斗加入,使用时,让稀盐酸与石灰石接触,反应开始,产生气体;不用时,可把导气管用止水夹夹住,产生的气体不能导出试管,造成试管内气体越来越多,压强越来越大,液体被压到长颈漏斗中,固体和液体分离,反应停止.所以可以随时控制反应的发生与停止;
故答案为:长颈漏斗;乙;
(2)二氧化碳和紫色石蕊试液中的水反应生成碳酸,碳酸是一种酸,可以使紫色石蕊溶液变红色,其反应的化学方程式为:H2O+CO2=H2CO3;
故答案为:H2O+CO2=H2CO3;
(3)氢气密度比空气的密度小,不能利用装置C收集氢气,故答案为:不能;氢气密度比空气的密度小.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
相关题目
14.一定质量的氧化铜及氧化铁分别跟足量的H₂反应.得到的固体质量相等,则氧化铜与氧化铁的质量之比为( )
| A. | 8:7 | B. | 7:8 | C. | 1:2 | D. | 2:1 |
11. 老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
(1)此气体是什么物质?验证它的实验方案如下:
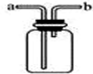
(2)如果用如图所示装置收集我猜想的气体,我认为气体应从a端(填“a”或“b”)导入.
 老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:
老师从实验桌上拿出两瓶常用的但标签已经模糊不清的试剂,分别是固体和液体,他取少量试剂在试管中混合,立即产生一种无色气体.我们对此气体展开了一系列探究:(1)此气体是什么物质?验证它的实验方案如下:
| 猜 想 | 验证猜想的实验步骤 | 现象及结论 |
| 我认为此气体可能是氧气 | 把带火星的木条伸入集气瓶中 | 木条复燃,证明该气体是氧气 |
| 产生此气体的一个化学方程式是2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑ | ||
8.对物质进行分类是学习化学的一种方法.下列物质属于纯净物的是( )
| A. | 啤酒 | B. | 石灰石 | C. | 液氧 | D. | 海水 |
12.要验证Zn.Fe.Cu三种金属的活动性强弱,最好的一组试剂是( )
| A. | Fe、CuSO4溶液、ZnSO4溶液 | B. | Cu、FeCl2溶液、ZnCl2溶液 | ||
| C. | Zn、FeSO4溶液、CuSO4溶液 | D. | Fe、Cu、Zn(NO3)2溶液 |
 某科学兴趣小组成员在查阅资料时了解到:牙膏除主要活性成分外,还有约占牙膏成分50%的CaCO3[或Si02、Al(OH)3、CaHP04]等摩擦剂和保持牙膏湿润的甘油等物质.于是对自己牙膏中的摩擦剂是什么产生了兴趣.
某科学兴趣小组成员在查阅资料时了解到:牙膏除主要活性成分外,还有约占牙膏成分50%的CaCO3[或Si02、Al(OH)3、CaHP04]等摩擦剂和保持牙膏湿润的甘油等物质.于是对自己牙膏中的摩擦剂是什么产生了兴趣. CO2是一种宝贵的碳氧资源.
CO2是一种宝贵的碳氧资源.