题目内容
7.烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g,某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如表:| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(2)参加反应的NaOH溶液的总质量是多少克?(要求写出计算过程)
分析 向硫酸和硫酸铜的混合溶液滴加氢氧化钠溶液,硫酸、硫酸铜都可与氢氧化钠发生反应,由于硫酸的存在氢氧化钠与硫酸铜不能生成氢氧化铜沉淀,待硫酸反应完才能产生氢氧化铜沉淀;所以记录数据中,加入50.0g氢氧化钠溶液时产生沉淀的质量为0;而在加入氢氧化钠溶液200.0g以后沉淀质量不再变化,说明硫酸铜也已完全反应,故生成沉淀量最大值为9.8g;
根据硫酸铜与氢氧化钠反应的化学方程式,由沉淀氢氧化铜的质量可计算混合溶液中硫酸铜的质量及与硫酸铜发生反应的氢氧化钠的质量.
解答 解:(1)由记录数据表可知,至硫酸铜完全反应共生成蓝色沉淀9.8g;Cu(OH)2----CuSO4
根据化学变化前后元素质量不变,混合溶液中硫酸铜的质量=$\frac{9.8g×\frac{64}{98}×100%}{\frac{64}{160}×100%}$=16.0g;
故答案为:9.8;16.0;
(2)设与硫酸反应的氢氧化钠的质量为x,与硫酸铜反应的氢氧化钠的质量为y
H2SO4+2NaOH═Na2SO4+2H2O
98 80
9.8g x
$\frac{98}{80}=\frac{9.8g}{x}$
x=8.0g
CuSO4+2NaOH═Cu(OH)2↓+Na2SO4
80 98
y 9.8g
$\frac{80}{98}=\frac{y}{9.8g}$
y=8g
故参加反应的氢氧化钠溶液的质量=$\frac{8g+8g}{10%}$=160g
答:参加反应的NaOH溶液的总质量是160g
点评 学生应熟悉利用化学方程式计算的思路和格式,能利用恰好反应及元素守恒和分析数据来解答.

练习册系列答案
相关题目
8.下列物质由离子构成的是( )
| A. | Cu | B. | MgCl2 | C. | CO2 | D. | C |
9.把pH=3的溶液与pH=6的溶液充分混合,所得溶液的pH值可能是( )
| A. | 2 | B. | 5 | C. | 9 | D. | 无法确定 |
15.如图1图象和表格是数据表达的重要手段,根据下列图表回答问题.
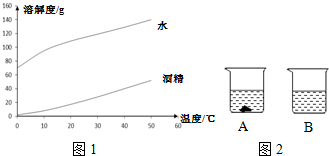
表一 甲、乙分别在水、酒精中的溶解度
图2 甲分别在水、酒精中的溶解度曲线
(1)分析表一数据可知,物质的溶解度受BCD(填序号)的影响.
A.溶剂质量B.溶剂性质C.溶质性质D.温度
(2)比较表一、图1可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点有AC(填序号).
A.数据更齐全B.数据更精准C.变化规律更直观
(3)若甲是NaOH,乙是Na2CO3,40℃时将CO2通入饱和的NaOH的酒精溶液,结合表一,写出该过程发生反应的化学方程式CO2+2NaOH═Na2CO3↓+H2O.
(4)40℃时,向两个盛有相同质量甲固体的烧杯中分别加入100g水和100g酒精,充分溶解后恢复至20℃,其结果如图2所示.下列说法中正确的是③(填序号).
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.

表一 甲、乙分别在水、酒精中的溶解度
| 甲 | 乙 | |||
| 20℃ | 40℃ | 20℃ | 40℃ | |
| 水 | 109g | 129g | 21.8g | 49g |
| 酒精 | 17.3g | 40g | 不溶 | 不溶 |
(1)分析表一数据可知,物质的溶解度受BCD(填序号)的影响.
A.溶剂质量B.溶剂性质C.溶质性质D.温度
(2)比较表一、图1可知,图象与表格均能反映温度对固体物质溶解度的影响,其中图象的优点有AC(填序号).
A.数据更齐全B.数据更精准C.变化规律更直观
(3)若甲是NaOH,乙是Na2CO3,40℃时将CO2通入饱和的NaOH的酒精溶液,结合表一,写出该过程发生反应的化学方程式CO2+2NaOH═Na2CO3↓+H2O.
(4)40℃时,向两个盛有相同质量甲固体的烧杯中分别加入100g水和100g酒精,充分溶解后恢复至20℃,其结果如图2所示.下列说法中正确的是③(填序号).
①烧杯B中一定是不饱和溶液.
②烧杯B中的溶剂是酒精.
③升高温度或增加溶剂都有可能将A中固体全部溶解.
④若将烧杯A中溶液变为不饱和溶液,溶液中溶质质量分数一定减小.
2. 溶液在生命活动和生产、生活中都起到十分重要的作用.
溶液在生命活动和生产、生活中都起到十分重要的作用.
(1)将下面调味品加入水中,不能形成溶液的是DA.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为酒精.(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
①实验a、b、c、d中,有未被溶解的KNO3固体析出的实验是e(填写实验编号).
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c<d(填“<”、“>”或“=”).
④取实验d所得溶液,若使其质量分数变为30%,在不改变温度的情况下,可以采取的操作是加入78.3克水.
(4)在不同温度时某物质A的溶解度如上表:根据表中信息,判断下列说法不正确的是D.
A.20℃时,A的溶解度为0.16g
B.40℃时,升高A的饱和溶液温度会析出溶质
C.60℃时,向100g水中加入0.20gA充分搅拌,固体不能完全溶解
D.A的溶解度随温度的升高而增大
(5)如图是一瓶开启的“XX牌”碳酸饮料的示意图,请回答:
开启时,大量的气泡从罐内冒出,说明随着压强的减小,气体的溶解度减小.
(6)实验室配制质量分数4%的氯化钠溶液50g,需要固体氯化钠的质量为2g,用量筒量取48mL水(水的密度1g/cm3).
(7)若用质量分数为8%的氯化钠溶液配制50g质量分数为4%的氯化钠溶液,要8%的氯化钠溶液的质量为25g.
 溶液在生命活动和生产、生活中都起到十分重要的作用.
溶液在生命活动和生产、生活中都起到十分重要的作用.(1)将下面调味品加入水中,不能形成溶液的是DA.食盐 B.蔗糖 C.味精 D.芝麻油
(2)碘酒中的溶剂为酒精.(写出物质名称)
(3)在一定温度下,向质量均为50g的4份水中分别加入一定量的KNO3固体,搅拌至充分溶解,(如有不溶的KNO3固体用过滤的方法除去),得到溶液.加入KNO3固体的质量与所得溶液的质量如下表:
| 实验编号 | a | b | c | d | e |
| 加入KNO3固体的质量 | 40 | 45 | 50 | 55 | 60 |
| 所得溶液质量 | 90 | 95 | 100 | 105 | 105 |
②该温度下KNO3的溶解度是110g.
③实验a、b、c、d所得溶液中质量分数大小关系为:a<b<c<d(填“<”、“>”或“=”).
④取实验d所得溶液,若使其质量分数变为30%,在不改变温度的情况下,可以采取的操作是加入78.3克水.
| 温度/ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 0.18 | 0.16 | 0.14 | 0.11 | 0.09 |
A.20℃时,A的溶解度为0.16g
B.40℃时,升高A的饱和溶液温度会析出溶质
C.60℃时,向100g水中加入0.20gA充分搅拌,固体不能完全溶解
D.A的溶解度随温度的升高而增大
(5)如图是一瓶开启的“XX牌”碳酸饮料的示意图,请回答:
开启时,大量的气泡从罐内冒出,说明随着压强的减小,气体的溶解度减小.
(6)实验室配制质量分数4%的氯化钠溶液50g,需要固体氯化钠的质量为2g,用量筒量取48mL水(水的密度1g/cm3).
(7)若用质量分数为8%的氯化钠溶液配制50g质量分数为4%的氯化钠溶液,要8%的氯化钠溶液的质量为25g.

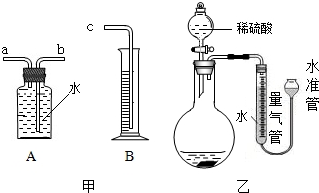

 硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示.
硝酸银溶液见光易分解,因此需要保存在棕色的试剂瓶中,为测定实验室中一瓶久置的AgNO3溶液中溶质的质量分数,取50g该溶液,并向其中加入NaCl溶液,测定结果如图所示.