题目内容
1.标出下列各组物质中加点元素的化合价(1)H2$\underset{S}{•}$ $\underset{S}{•}$ $\underset{S}{•}$ O2 Na2$\underset{S}{•}$ O3 H2$\underset{S}{•}$ O4
(2)$\underset{Mn}{•}$O2 $\underset{Mn}{•}$Cl2 $\underset{Mn}{•}$ Ca$\underset{Mn}{•}$O4 K$\underset{Mn}{•}$O4.
分析 根据单质中元素的化合价为0、在化合物中正负化合价代数和为零,结合各化学式计算出化合价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,进行分析解答.
解答 解:(1)氢元素显+1价,设硫元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x=0,则x=-2价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫化氢中硫元素显-2价可表示为:${H}_{2}\stackrel{-2}{S}$.
根据单质中元素的化合价为0,S属于单质,故硫元素的化合价为0;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫中硫元素的化合价为0可表示为:$\stackrel{0}{S}$.
氧元素显-2价,设硫元素的化合价是y,可得:y+(-2)×2=0,则y=+4价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故二氧化硫中硫元素显+4价可表示为:$\stackrel{+4}{S}{O}_{2}$.
钠元素显+1价,氧元素显-2价,设硫元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:(+1)×2+z+(-2)×3=0,则z=+4价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故亚硫酸钠中硫元素显+4价可表示为:Na2$\stackrel{+4}{S}$O3.
氢元素显+1价,氧元素显-2价,设硫元素的化合价是m,根据在化合物中正负化合价代数和为零,可得:(+1)×2+m+(-2)×3=0,则m=+4价;由化合价的表示方法,在其化学式该元素的上方用正负号和数字表示,正负号在前,数字在后,故硫酸中硫元素显+4价可表示为:H2$\stackrel{+6}{S}$O4.
故填:${H}_{2}\stackrel{-2}{S}$;$\stackrel{0}{S}$;$\stackrel{+4}{S}{O}_{2}$;Na2$\stackrel{+4}{S}$O3;H2$\stackrel{+6}{S}$O4.
(2)氧显-2价,氯显-1价,钾显+1价,根据单质中元素的化合价为0、在化合物中正负化合价代数和为零可知,二氧化锰、氯化锰、锰、锰酸钙、高锰酸钾中锰元素的化合价分别为+4、+2、0、+6、+7,故填:
$\stackrel{+4}{Mn}{O}_{2}$、$\stackrel{+2}{Mn}{Cl}_{2}$、$\stackrel{0}{Mn}$、Ca$\stackrel{+6}{Mn}$O4、K$\stackrel{+7}{Mn}$O4.
点评 本题难度不大,掌握化合价的表示方法、利用化合价的原则(化合物中正负化合价代数和为零)计算指定元素的化合价的方法即可正确解答本题.

| A. | 48克 | B. | 32克 | C. | 24克 | D. | 40克 |
| A. | 氢氧化钠粉末 | B. | 浓盐酸 | C. | 氧化铁 | D. | 氯化钠晶体 |
| A. | 改变能源结构,发展太阳能、核能、水能、以代替化石燃料 | |
| B. | 用石灰水吸收空气中的CO2 | |
| C. | 限制汽车工业的发展,减少汽车数量 | |
| D. | 大量滥砍乱伐,减少绿化面积 |
| A. | 河水 | B. | 海水 | C. | 蒸馏水 | D. | 矿泉水 |
| A. | 二氧化锰 | B. | 高锰酸钾 | C. | 氧化铜 | D. | 液氧 |
| A. | 硫 | B. | 汞 | C. | 铜 | D. | 铁 |
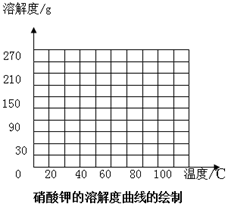 硝酸钾在不同温度时的溶解度如下:
硝酸钾在不同温度时的溶解度如下:| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |