题目内容
5.有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成.为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:
请分析实验过程,回答下列问题:
(1)白色粉末中一定不含CuSO4、Na2SO4;可能含有NaOH.
(2)生成白色沉淀的化学方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】
猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取无色滤液少许于试管中,滴加过量的BaCl2溶液 | 产生白色沉淀 | 猜想Ⅱ不成立 |
| ②在①反应后的试管中滴加无色酚酞溶液 | 溶液变为红色 | 猜想Ⅲ成立 |
分析 根据硫酸铜在溶液中显蓝色,硫酸钠和氯化钡生成不溶于酸的硫酸钡沉淀,碳酸钠和氯化钡生成溶于酸的碳酸钡沉淀,氢氧化钠、碳酸钠的水溶液显碱性等知识进行分析.
解答 解:硫酸铜在溶液中显蓝色,硫酸钠和氯化钡生成不溶于酸的硫酸钡沉淀,碳酸钠和氯化钡生成溶于酸的碳酸钡沉淀,氢氧化钠、碳酸钠的水溶液显碱性.
(1)白色粉末加水溶解得到无色溶液和白色沉淀,所以粉末中一定不含硫酸铜,白色沉淀加入稀盐酸,全部溶解,所以白色粉末中一定含有氯化钡、碳酸钠,一定不含硫酸钠,可能含有氢氧化钠;
(2)生成白色沉淀的反应是碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl;
(3)碳酸钠、氢氧化钠都显碱性,都能使无色酚酞变红色,要检验氢氧化钠需要先将碳酸钠检验并除去,所以
| 实验步骤 | 实验现象 | 实验结论 |
| ①取无色滤液少许于试管中,滴加过量的BaCl2溶液 | 产生白色沉淀 | 猜想Ⅱ不成立 |
| ②在①反应后的试管中滴加无色酚酞溶液 | 溶液变为红色 | 猜想Ⅲ成立 |
故答案为:(1)CuSO4、Na2SO4,NaOH;
(2)Na2CO3+BaCl2=BaCO3↓+2NaCl;
(3)【进行实验】无色酚酞溶液;
【探究结论】Na2CO3、BaCl2、NaOH.
点评 在解此类题时,首先分析题中所给物质的性质和两两之间的反应,然后依据题中的现象判断各物质的存在性,最后进行验证即可.

练习册系列答案
相关题目
15.下列各组物质的溶液不用其他试剂就可鉴别出来的是( )
| A. | HCl CuCl2 NaNO3 Na2SO4 | B. | BaCl2 Na2CO3 HCl (NH4)2CO3 | ||
| C. | FeCl3 HCl NaCl NaOH | D. | Na2CO3 Na2SO4 HCl H2SO4 |
13.下列数据为常见水果的近似pH,其中酸性最强的是( )
| A. | 杨梅pH=2.5 | B. | 苹果pH=4.1 | C. | 菠萝pH=5.1 | D. | 柿子pH=8.5 |
17.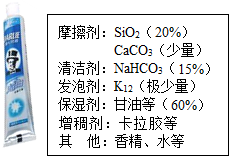 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
【资料卡片】:
a、SiO2不溶于水、且不与酸反应,高温不分解;
b、NaHCO3受热易分解,生成Na2CO3、H2O、CO2;
c、牙膏中保湿剂、增稠剂、香精等均为有机物.
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得其上层清液的pH为8.3,则此牙膏显弱碱性性,实验室能否用pH试纸测得该数值,请你作出判断并说明理由.不能,因为pH试纸只能测定出整数值;
(2)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的K12(一种钠盐)析出,则K12的溶解度和温度的关系是K12的溶解度随温度降低而降低(或随温度升高而增大);
(3)为测定此牙膏中SiO2的质量分数,兴趣小组同学设计了如下方案,并进行了3次实验:
【实验步骤】:
①准确称取2.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀HCl,至气体不再产生为止;
③过滤、洗涤、称量得到剩余固体质量(如表);
④根据实验数据进行计算.
【数据处理】:
(4)此测定做3次实验的目的是提高实验的精确度(或可信度);
(5)综合上述实验方案及实验数据,计算此牙膏中SiO2的质量分数.22%;
【实验分析】:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)高温加热的目的除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)步骤②中,加稀HCl发生的反应有CaO+2HCl═CaCl2+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(9)步骤③中,洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液;若不洗涤,则测定结果将偏大.(填“偏大”、“偏小”或“不变”)
(10)为保证洗涤效果,最好用A洗涤.
A.蒸馏水 B.自来水 C.饱和NaCl溶液 D.饱和CaCl2溶液.
 牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:
牙膏是生活必需品,某兴趣小组同学对某品牌市售牙膏展开如下探究,请回答问题:【资料卡片】:
a、SiO2不溶于水、且不与酸反应,高温不分解;
b、NaHCO3受热易分解,生成Na2CO3、H2O、CO2;
c、牙膏中保湿剂、增稠剂、香精等均为有机物.
(1)取一小段牙膏,加入蒸馏水,充分搅拌后静置,测得其上层清液的pH为8.3,则此牙膏显弱碱性性,实验室能否用pH试纸测得该数值,请你作出判断并说明理由.不能,因为pH试纸只能测定出整数值;
(2)小岳同学发现,此品牌牙膏在冬季会出现颗粒变大的现象.资料显示是牙膏中的K12(一种钠盐)析出,则K12的溶解度和温度的关系是K12的溶解度随温度降低而降低(或随温度升高而增大);
(3)为测定此牙膏中SiO2的质量分数,兴趣小组同学设计了如下方案,并进行了3次实验:
【实验步骤】:
①准确称取2.0g牙膏膏体,烘干水分,高温加热,至质量不再减轻为止,在干燥器中冷却至室温;
②转移剩余物至烧杯中,加入稀HCl,至气体不再产生为止;
③过滤、洗涤、称量得到剩余固体质量(如表);
| 实验编号 | 1 | 2 | 3 |
| 实验前(g) | 2.00 | 2.00 | 2.00 |
| 试验后(g) | 0.43 | 0.44 | 0.45 |
【数据处理】:
(4)此测定做3次实验的目的是提高实验的精确度(或可信度);
(5)综合上述实验方案及实验数据,计算此牙膏中SiO2的质量分数.22%;
【实验分析】:
(6)按上述实验步骤操作,发现测定结果偏大,导致偏大的原因可能是步骤③中,没有将剩余固体进行干燥,有洗涤液附着在固体表面;
(7)高温加热的目的除为了除去CaCO3及NaHCO3以外,还为除去保湿剂、增稠剂、香精等有机物;
(8)步骤②中,加稀HCl发生的反应有CaO+2HCl═CaCl2+H2O、Na2CO3+2HCl═2NaCl+H2O+CO2↑;
(9)步骤③中,洗涤的目的是除去固体表面附着的CaCl2和NaCl溶液;若不洗涤,则测定结果将偏大.(填“偏大”、“偏小”或“不变”)
(10)为保证洗涤效果,最好用A洗涤.
A.蒸馏水 B.自来水 C.饱和NaCl溶液 D.饱和CaCl2溶液.
14.下列模型能表示氧气分子结构的是( )
| A. | 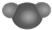 | B. |  | C. | 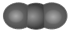 | D. | 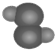 |
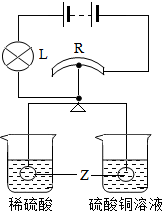 如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠杆的中央且可以随杠杆左右移动.杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将锌球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到:
如图所示,R是滑动变阻器,它的金属滑片垂直固定在等臂金属杠杆的中央且可以随杠杆左右移动.杠杆两端分别悬挂等质量、等体积的金属锌球,此时杠杆平衡.再将锌球同时分别浸没到密度相同的稀硫酸和硫酸铜溶液中.反应一段时间后会观察到: 今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.
今年我国纪念“世界水日”和“中国水周”活动的宣传主题为“节约水资源,保障水安全”.