��Ŀ����
��1����֪����ͭ��Һ������������Һ��Ӧ�õ���ɫ����������������ֳ���������һ�ֺ�ɫ�����ʣ�����д�����е�������ѧ��Ӧ����ʽ ��
��
��2�����еij�����ѧ��ȤС���ͬѧ�������ʵ�飺���Թ��е���2ml��CuSO4��Һ���ټ���һ������NaOH��Һ��Ӧ��õ��ij�����������ɫ�ģ�����dz��ɫ�ģ�Ȼ���ֽ�����Һ���������ڣ��۲첻���зֽ�������CuO�ļ�������ͨ���������ϵ�֪��dz��ɫ�ij�����Ϊ�ܽ�ȼ�С�ļ�ʽ����ͭ[Cu4(OH)6SO4]��
��д������dz��ɫ�����Ļ�ѧ����ʽ��
���������ʵ��֤�������к����������д��ʵ�鷽��������
��
��1��CuSO4+2NaOH==Cu(OH)2��+Na2SO4 ��Cu(OH)2====CuO+H2O
��2��4CuSO4+6NaOH==Cu4(OH)6SO4��+3Na2SO4
ȡ������������ϡ����Ȼ������ᱵ���а�ɫ�������ɡ�

| ����NaOH��Һ������/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| ���ɳ���������/g | 0.0 | 2.45 | 8.6 | 9.8 | 9.8 |
��2���μӷ�Ӧ��NaOH��Һ���������Ƕ��ٿˣ���Ҫ��д��������̣�
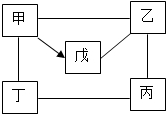 �ס��ҡ�����������ֱ���ϡ���ᡢþ������������Һ������þ������ͭ��Һ�е�һ�֣�
�ס��ҡ�����������ֱ���ϡ���ᡢþ������������Һ������þ������ͭ��Һ�е�һ�֣�