题目内容
某兴趣小组用图所示流程制取氧气,并回收提纯氧化钾和二氧化锰
回答下列问题:
(1)根据化学式计算,理论上可制得氧气的质量是多少?(反应物中的氧元素可全部转化成氧气,写出计算过程
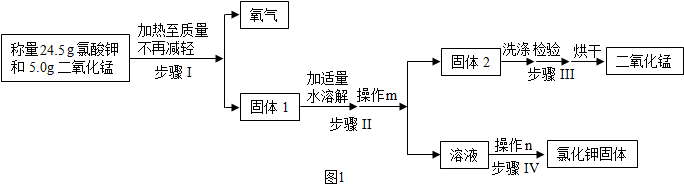
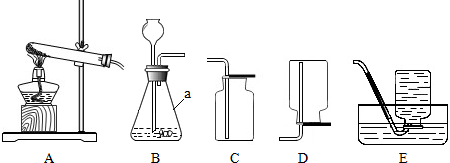
(2)①写出图乙中仪器a、b的名称
a ;b .
②步骤Ⅱ中的操作m应选择图2中 (填“甲”或“乙”)装置,该操作中玻璃棒的作用是 .

③进行图甲实验,在制作过滤器时候若发现滤纸不能紧贴漏斗内壁,应进行的操作是 .
A.将滤纸截取部分 B.直接进行下一步操作
C.改变滤纸第一次折叠的角度 D.改变滤纸第二次折叠的角.
回答下列问题:
(1)根据化学式计算,理论上可制得氧气的质量是多少?(反应物中的氧元素可全部转化成氧气,写出计算过程

(2)①写出图乙中仪器a、b的名称
a
②步骤Ⅱ中的操作m应选择图2中

③进行图甲实验,在制作过滤器时候若发现滤纸不能紧贴漏斗内壁,应进行的操作是
A.将滤纸截取部分 B.直接进行下一步操作
C.改变滤纸第一次折叠的角度 D.改变滤纸第二次折叠的角.
考点:混合物的分离方法,过滤的原理、方法及其应用,蒸发与蒸馏操作,化合物中某元素的质量计算
专题:物质的分离和提纯
分析:根据化学式计算氧气的质量,据图即可写出有关仪器的名称;根据过滤操作的注意事项进行分析解答即可.
解答:解:(1)氯酸钾中的氧元素全部转化生成氧气,故氯酸钾中氧元素的质量就是生成的氧气的质量,故填:24.5g×
=9.6g;
(2)①据图可以知道,a是铁架台,b是酒精灯,故填:铁架台,酒精灯;
②经过步骤Ⅱ得到了固体和液体,故是过滤操作,该操作中玻璃棒的作用是引流,故填:甲,引流;
③在制作过滤器时候若发现滤纸不能紧贴漏斗内壁,可以改变滤纸第二次折叠的角,故填:D.
| 48 |
| 122.5 |
(2)①据图可以知道,a是铁架台,b是酒精灯,故填:铁架台,酒精灯;
②经过步骤Ⅱ得到了固体和液体,故是过滤操作,该操作中玻璃棒的作用是引流,故填:甲,引流;
③在制作过滤器时候若发现滤纸不能紧贴漏斗内壁,可以改变滤纸第二次折叠的角,故填:D.
点评:本题考查了物质的分离和有关化学式的计算,完成此题,可以依据已有的知识进行.

练习册系列答案
 小题狂做系列答案
小题狂做系列答案
相关题目
下列除去杂质方法中,错误的一组是( )
| 选项 | 待提纯的物质 | 杂质 | 除去杂质的方法 |
| A | CaCl2溶液 | HCl | 过量CaCO3、过滤 |
| B | NaOH溶液 | Ca(OH)2 | 过量Na2CO3溶液、过滤 |
| C | Cu | Mg | 稀硫酸、过滤 |
| D | CH4 | H2O | 通过盛浓硫酸的洗气瓶 |
| A、A | B、B | C、C | D、D |
下列有关溶液的计算说法不正确的是( )
| A、在某温度下,将35g KCl溶液蒸干得到7gKCl固体,则原溶液溶质质量分数为20% |
| B、把100g 98%浓硫酸稀释至10%稀硫酸,外加水的质量为880g |
| C、把50g10% NaCl溶液变为20%的NaCl溶液,需蒸发掉25g水 |
| D、在20℃时将40g KNO3充分溶解在100g水中,仍然有8.4g KNO3不溶.所得溶液中KNO3质量分数是31.6% |
下列说法不正确的是( )
| A、实验室里常用稀盐酸与大理石反应来制取少量二氧化碳气体 |
| B、“电解水实验”表明水是由氢元素和氧元素组成的 |
| C、铁丝在空气中剧烈燃烧,火星四射,生成黄色固体,放出大量的热 |
| D、资料介绍,成年人缺钙易得软骨病,这里的“钙”是指钙元素 |
正确的化学实验操作对实验结果、人身安全非常重要.如图中的实验操作正确的是( )
A、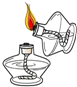 点燃酒精灯 |
B、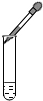 滴加液体 |
C、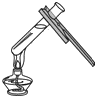 加热液体 |
D、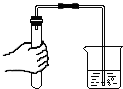 检查气密性 |
下列关于分子和原子的说法不正确的是( )
| A、分子在不停地运动 |
| B、分子在化学反应前后种类和数目保持不变 |
| C、原子可以直接构成物质 |
| D、原子是化学变化中的最小粒子 |
某学生用托盘天平称量17.5g食盐(1g以下用游码),错误地把食盐与砝码的位置颠倒,此时他称得的食盐的实际质量为( )
| A、18.0g |
| B、17.0g |
| C、16.5g |
| D、18.5g |
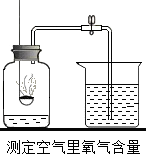 物质在空气中燃烧,多数只与氧气反应,也有不同的,如镁在空气中燃烧不仅与氧气反应,还与氮气和二氧化碳反应.如图是测定空气中燃烧氧气含量的装置图,燃烧匙内放入红磷,测得氧气约占空气总体积的
物质在空气中燃烧,多数只与氧气反应,也有不同的,如镁在空气中燃烧不仅与氧气反应,还与氮气和二氧化碳反应.如图是测定空气中燃烧氧气含量的装置图,燃烧匙内放入红磷,测得氧气约占空气总体积的