题目内容
【题目】金属材料在日常生活及工农业生产中具有广泛的应用。请你回答以下问题:
(1)下列金属制品中,利用金属导热性的是_____;
A 金属硬币 B 铝制导线 C 铜制火锅
(2)工业上用赤铁矿石炼铁的化学方程式是_____;
(3)用稀硫酸除铁锈的现象为_____;
(4)在试管中放入一根去除氧化膜的镁条,向其中加入硝酸银溶液至浸没镁条,观察到如下现象:①镁条表面迅速覆盖一层疏松的固体物质,②镁条表面有明显的气泡冒出,经检验发现生成的固体物质中有单质银;生成的气泡中有氢气;对于上述实验现象的分析错误的是 _____。
A 镁能从硝酸银溶液中置换出银
B 该实验可判断银能置换出酸中的氢
C 硝酸银溶液可能显酸性
D 溶液中只发生2AgNO3+Mg=Mg(NO3)2+2Ag的反应
【答案】C 3CO+Fe2O3 2Fe+3CO2 铁锈逐渐消失,溶液由无色变为黄色(不答全不得分) B,D
2Fe+3CO2 铁锈逐渐消失,溶液由无色变为黄色(不答全不得分) B,D
【解析】
(1)A.金属硬币是利用了金属的耐腐蚀、硬度大、美观好看等性质,故A错误;
B.铝制导线是利用了铝的导电性,故B错误;
C.铜制火锅是利用金属导热性,故C正确;故选C。
(2)工业上是利用氧化铁和一氧化碳反应的原理进行冶铁,化学方程式为:Fe2O3+3CO![]() 2Fe+2CO2;
2Fe+2CO2;
(3)铁锈的主要成分是氧化铁,氧化铁和稀硫酸反应生成硫酸铁和氢气,硫酸铁溶液是黄色的;
(4)A.在金属活动性顺序中,镁在银的前面,能把银从硝酸银溶液中给置换出来,故A正确;
B.在金属活动性顺序里,银在氢的后面,无法置换出酸中的氢,故B错误;
C.在金属活动性顺序中,镁在氢的前面,能置换出酸中的氢,因为生成的气泡中有氢气,所以硝酸银溶液可能显酸性,故C正确;
D.溶液中除了发生2AgNO3+Mg=Mg(NO3)2+2Ag的反应还有镁和酸的反应,故D错误。故选BD。

 阅读快车系列答案
阅读快车系列答案【题目】某兴趣小组对KCIO3分解反应的催化剂进行研究,在相同的加热条件下,用如图装置完成表中实验:
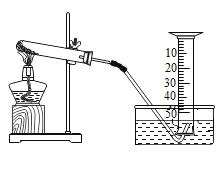
编号 | KCIO3质量/g | 催化剂 | 催化剂质量/g | 收集50 mLO2所需时间/s |
实验1 | 5 | 一 | 一 | 171 |
实验2 | 5 | MnO2 | 0.5 | 49 |
实验3 | 5 | Fe2O3 | 0.5 | 58 |
实验4 | 5 | KCl | 0.5 | 154 |
(1)设置实验1的目的是_____________。
(2)表中所列3种催化剂的催化效果最佳的是___________________。
(3)写出KCIO3分解的化学方程式:________________。
(4)由实验1和实验4可知,KC1_______________ (填“有"或“无”)催化作用。
(5)要比较KCIO3分解反应中不同催化剂的催化效果,除了测量收集50 mLO3所需时间外,还可以测量相同时间内______________。
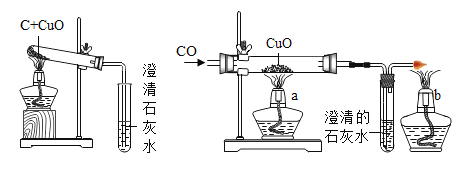
【题目】化学小组用如图图所示装置进行木炭和氧化铜反应的实验
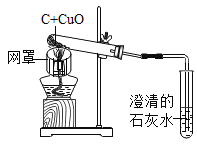
查阅资料:①氧化铜和稀硫酸充分反应后生成硫酸铜和水
②氢氧化钠(NaOH)溶液能和二氧化碳后应,且无明显现象
在进行实验时,他们首先将碳和氧化铜碾成粉末,且混合均匀后,再开始实验,这样做的目的是______________________________;充分反应后,化学小组的同学对试管内的固体成分进行了探究Ⅰ,对生成气体的成分进行了探究II,按要求填空。
探究I:试管内固体的成分是什么?
(作出猜想)
猜想一:Cu 猜想二: _______________; 猜想三:Cu和CuO
(实验验证)
实验操作 | 实验现象 | 实验结论 |
取少量的固体加入试管中,然后加入过量稀硫酸,振荡 | _____________。 | 猜想三成立 |
探究II:生成的气体中是否含有一氧化碳?
通过上面的实验分析,生成的气体中一定含有二氧化碳,是否含有一氧化碳,小组同学进行了下列实验
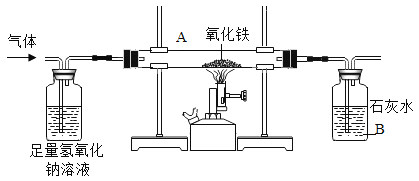
实验操作 | 实验现象 | 结论 |
收集碳和氧化铜反应后产生的气体,再将气体通入上面装置中 | _____________________________________________________。 | 生成的气体中有一氧化碳 |
则B中石灰水的作用是________,A中反应的化学方程式为____________。
(实验反思)从环保的角度思考,该装置的缺陷是___________。