题目内容
2.完成下列反应的化学方程式,并回答有关问题.(1)工业上用赤铁矿在高温条件下炼铁的原理:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,冶炼生铁的设备是高炉;
(2)检验二氧化碳,将二氧化碳气体通入饱和石灰水:Ca(OH)2+CO2═CaCO3↓+H2O,反应后溶液不饱和(选填“饱和”或“不饱和”);
(3)氯化铵晶体和熟石灰混合研磨会生成一种氨臭味的气体:2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑,检验该气体可用湿润的红色石蕊试纸;
(4)用氨水中和硫酸厂排出来的废水:2NH3•H2O+H2SO4=(NH4)2SO4+2H2O,过程中废水的pH变大(选填“变大”或“变小”);
(5)美剧《越狱》中迈克为了用硫酸腐蚀医务室下水道用于逃生,于是用磷酸和硫酸钙反应制得磷酸钙沉淀和硫酸:2H3PO4+3CaSO4=Ca3(PO4)2+3H2O,这个反应属于复分解反应类型.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写;再根据反应来分析相关问题.
解答 解:(1)工业上用一氧化碳还原氧化铁炼铁,主要是利用CO的还原性,在高温下和氧化铁反应生成铁和二氧化碳,反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;冶炼生铁的主要设备是高炉.故填:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;高炉;
(2)二氧化碳与氢氧化钙反应生成碳酸钙和水,故石灰水变浑浊,用来检验二氧化碳,方程式为:Ca(OH)2+CO2═CaCO3↓+H2O,此时所得溶液为氢氧化钙的不饱和溶液;故填:Ca(OH)2+CO2═CaCO3↓+H2O;不饱和;
(3)氯化铵晶体(NH4Cl)和熟石灰混合研磨生成一种氨臭味的气体(氨气),反应的化学方程式是:2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑;氨气能使红色石蕊试纸变蓝色,因此可以用湿润的红色石蕊试纸来检验氨气;故答案为:2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑;湿润的红色石蕊;
(4)氨水中和废水中的稀硫酸生成硫酸铵和水,反应的化学方程式是:2NH3•H2O+H2SO4=(NH4)2SO4+2H2O.酸的pH小于7,加入pH大于7的氨水调节至中性,pH=7,此过程中溶液的pH变大;故填:2NH3•H2O+H2SO4=(NH4)2SO4+2H2O;变大;
(5)磷酸和硫酸钙反应制得磷酸钙沉淀和硫酸,反应的化学方程式为2H3PO4+3CaSO4=Ca3(PO4)2+3H2O,该反应是由两种化合物相互交换成分生成两种新的化合物,属于复分解反应,故填:2H3PO4+3CaSO4=Ca3(PO4)2+3H2O;复分解.
点评 本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

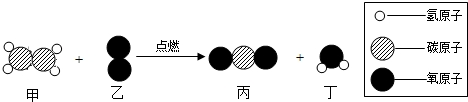
| A. | 该反应中有四种化合物 | |
| B. | 参加反应的甲、乙分子个数比为1:3 | |
| C. | 该反应属于置换反应 | |
| D. | 参加反应的甲、乙物质的质量比为28:32 |
| A. | Cl2、NaCl | B. | NH4Cl、HNO3 | C. | MnO2、K2MnO4 | D. | SO2、H2SO3 |
| A. | 天然气燃烧 | B. | 电解水制氢气 | C. | 核能发电 | D. | 干电池放电 |
| A. | 用托盘天平称得干燥精盐的质量为1.7g | |
| B. | 用广泛pH试纸测得某河水的pH为6.2 | |
| C. | 用50mL量筒准确量取8.5mL浓盐酸 | |
| D. | 将5.6g氧化钙投入94.4g水中,充分搅拌,配成质量分数为5.6%氢氧化钙溶液 |
| A. | 生石灰、氢氧化钙、Ca(OH)2 | B. | 水银、贡、Hg | ||
| C. | 纯碱、碳酸钠、NaCO3 | D. | 小苏打、碳酸氢钠、NaHCO3 |
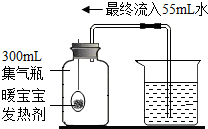 暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).
暖宝宝中的发热剂是铁粉、水和食盐等,发热剂能代替红磷测定空气中氧气含量(装置见图).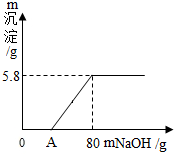 向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答:
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答: