题目内容
8.用符号和数字填空:①2个硫酸根离子2SO42-;
②3个氮气分子3N2;
③天然气的主要成分CH4;
④厨房调味中的盐NaCl.
分析 本题考查化学用语的意义及书写,解题关键是分清化学用语所表达的对象是分子、原子、离子还是化合价,才能在化学符号前或其它位置加上适当的计量数来完整地表达其意义,并能根据物质化学式的书写规则正确书写物质的化学式,才能熟练准确的解答此类题目.
解答 解:①离子的表示方法:在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其元素符号前加上相应的数字,两个硫酸根离子表示为2SO42-;
②由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则3个氮气分子可表示为:3N2.
③天然气的主要成分是甲烷,其化学式为:CH4;
④厨房调味中的盐是氯化钠,其化学式为:NaCl;
故答案为:①2SO42- ②3N2 ③CH4 ④NaCl
点评 本题主要考查学生对化学用语的书写和理解能力,题目设计既包含对化学符号意义的了解,又考查了学生对化学符号的书写,考查全面,注重基础,题目难度较易.

练习册系列答案
相关题目
16.下列结构示意图表示阳离子的是( )
| A. | 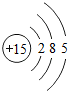 | B. | 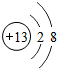 | C. | 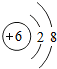 | D. | 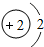 |
3.天热的时候,把半杯糖水(蔗糖已全部溶解)放进冰箱的冷藏室(水未结冰).过一段时间后杯底出现了部分晶体.对这一现象的认识正确的是( )
| A. | 析出晶体前后糖水中蔗糖的质量分数不变 | |
| B. | 析出晶体前糖水中蔗糖的质量分数比析出晶体后小 | |
| C. | 析出晶体后的糖水一定是饱和溶液 | |
| D. | 未放入冰箱前的糖水一定是饱和溶液 |
13.用分子的相关知识解释下列生活中的现象,其中错误的是( )
| A. | 热胀冷缩,说明分子的大小随温度升降而改娈 | |
| B. | “酒香不怕巷子深”,说明分子在不停地运动 | |
| C. | 10mL酒精和10mL水混合后,体积小于20mL,说明分子间有空隙 | |
| D. | 水通电分解生成氢气和氧气,说明分子在化学变化中可再分 |
17.某同学对CaH2的制备和性质进行探究.
【阅读资料】①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成一种碱和一种气体
③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.
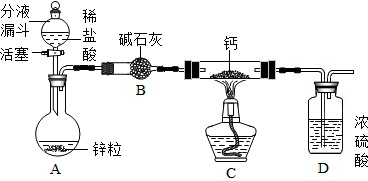
(1)装置B的作用是吸收水蒸气;装置D的作用是防止空气中的水蒸气与钙反应;
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显蓝色.该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是也可能是钙和水反应.
【CaH2的性质探究】
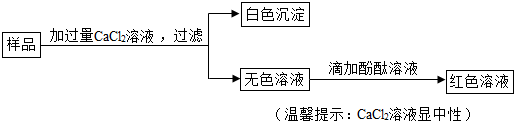
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.该同学进行了如下的探究.
(3)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为H2 (写化学式).
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3+2NaOH
【实验验证】
【定量分析】
取制得的CaH2样品1g(假设不含其他杂质)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2g,则该样品中CaH2的质量分数为84%.
【阅读资料】①用H2与钙加热制得CaH2
②钙遇水立即发生剧烈反应生成一种碱和一种气体
③CaH2要密封保存,遇水反应也生成一种碱和一种气体
【CaH2的制备】设计的制取装置如图所示.

(1)装置B的作用是吸收水蒸气;装置D的作用是防止空气中的水蒸气与钙反应;
(2)制备CaH2实验结束后,取少量产物,小心加入水中,观察有气泡产生,在溶液中滴入石蕊试液后显蓝色.该同学据此判断:实验中确有氢化钙生成,其他同学提出结论不一定正确,原因是也可能是钙和水反应.
【CaH2的性质探究】
取少量上述制得的CaH2 样品加入到足量的碳酸钠溶液中,产生大量气泡,过滤,得到滤渣和滤液.经检验滤渣的成分是碳酸钙.该同学进行了如下的探究.
(3)点燃产生的气体,火焰淡蓝色;将燃烧产物通入澄清石灰水中,无现象.则该气体为H2 (写化学式).
(4)对滤液中溶质的成分做出如下猜测并进行实验:
猜想一:NaOH 猜想二:NaOH、Ca(OH)2
猜想三:NaOH、Na2CO3 猜想四:NaOH、Na2CO3、Ca(OH)2
经过讨论,大家一致认为猜想四不合理,请用化学方程式说明原因Na2CO3+Ca(OH)2=CaCO3+2NaOH
【实验验证】
| 实验 | 现象 | 结论 |
| 实验一:取滤液,向其中滴入少量 Na2CO3溶液 | 无明显现象 | 猜想二不成立 |
| 实验二:另取滤液,向其中加入足量稀盐酸 | 过一会儿有气泡产生 | 猜想三成立 |
取制得的CaH2样品1g(假设不含其他杂质)加入到足量的Na2CO3溶液中,充分反应后,过滤、洗涤、干燥称得CaCO3质量为2g,则该样品中CaH2的质量分数为84%.
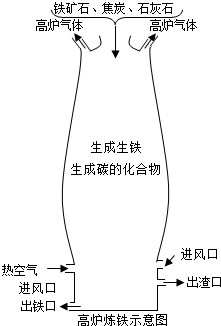 (1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.
(1)空气通过进风口与原料中的焦炭充分反应,其化学方程式为O2+C$\frac{\underline{\;点燃\;}}{\;}$CO2.