题目内容
13.在各种金属材料中铜是人类应用比较广泛的金属之一,某学习小组欲测定铜的相对原子质量,设计如下实验方案:实验步骤:①连接好装置 ②检查装置气密性 ③装入药品 ④打开分液漏斗活塞向锥形瓶中滴加入稀盐酸 ⑤一段时间后点燃酒精灯 ⑥D中黑色固体完全变成红色,停止加热,待D中玻璃管冷却至室温,关闭分液漏斗活塞 ⑦数据处理
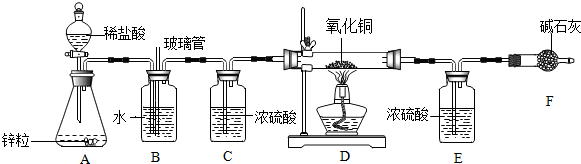
请回答下列问题:
(1)请补全实验步骤②检查装置气密性.
(2)B装置中水的作用吸收氯化氢气体,长玻璃管的作用平衡B装置内外的气压,
C装置的作用吸收水蒸气,D装置中反应方程式CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
(3)已知:CuO样品质量为m1克,E中增重为m2克,D中反应后固体质量为m3克,实际参加反应氢气的质量为m4克,试用m1,m2列出铜的相对原子质量的表达式$\frac{18{m}_{1}}{{m}_{2}}$-16.若无F装置,则对测定结果的影响偏小 (填“偏大”、“偏小”、“无影响”),以下数据还能测定铜的相对原子质量的是ABC.
A.m2 m3 B.m3 m4 C.m1 m4 D.m2 m4
(4)请你评价实验有什么不妥之处,并说明原因未与氧化铜反应的氢气,排放到空气中,应加尾气收集装置.
分析 (1)根据制取气体是先要检查装置的气密性进行分析;
(2)根据水可以吸收盐酸挥发的氯化氢气体,同时与长玻璃管起到缓冲压力的作用,浓硫酸具有吸水性,氢气和氧化铜在加热的条件下生成铜和水进行分析;
(3)根据CuO样品的质量,E中增重水的质量分析铜的相对原子质量;F装置阻止空气中的水蒸气浸入E装置,结合方程式只要能包含铜或氧化铜的质量数据,列比例式就可求解;
(4)根据实验中无法判断CuO是否完全反应进行分析.
解答 解:(1)制取气体是先要检查装置的气密性;
(2)B是安全瓶,B中气体压力过大时,水就会从玻璃管上端溢出,B中所盛是水,水的作用吸收盐酸挥发的氯化氢气体,浓硫酸具有吸水性,干燥氢气,氢气和氧化铜在加热的条件下生成铜和水,化学方程式为:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(3)设铜的相对原子质量为x
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
x+16 18
m1 m2
$\frac{x+16}{{m}_{1}}$=$\frac{18}{{m}_{2}}$
x=$\frac{18{m}_{1}}{{m}_{2}}$-16;
F装置阻止空气中的水蒸气浸入E装置,若无F装置,E中增重m2变大,则对测定结果偏小;结合方程式只要能包含铜或氧化铜的质量数据,列比例式就可求解,故选:ABC;
(4)实验中未与氧化铜反应的氢气,排放到空气中,应加尾气收集装置.
故答案为:(1)检查装置的气密性;
(2)吸收盐酸挥发的氯化氢气体;起安全作用,当B中气体压力过大时,水就会从玻璃管上端溢出;干燥氢气,H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(3)$\frac{18{m}_{1}}{{m}_{2}}$-16,偏小,ABC;
(4)未与氧化铜反应的氢气,排放到空气中,应加尾气收集装置.
点评 本题考查了实验室制氢气的原理以及根据反应的原理选择合适的实验装置,学生的平常的化学学习中一定要注重对双基知识的学习,只有具备完整的知识系统,才能够很好的解决综合问题.

| A. | 细铁丝在空气中剧烈燃烧,火星四射 | |
| B. | 硫在空气中燃烧,发出微弱的淡蓝色火焰,生成一种有刺激性气味的气体二氧化硫 | |
| C. | 磷在空气中燃烧,产生大量白色烟雾 | |
| D. | 木炭在空气中燃烧,发出红光,放出热量 |
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 55 | 4 | 5 | 2 |
| 反应后质量/g | X | 4 | 25 | 32 |
(2)下列说法中正确的是B.
A.乙一定是催化剂 B.甲是反应物.
| A. |  氧化钙溶液 | B. |  烧碱溶液 | C. |  胆矾溶液 | D. |  食盐溶液 |
【实验探究】
| 探 究 过 程 | 实 验 现 象 | 结论及化学方程式 | |
| K2CO3 | (NH4)2SO4 | ||
| (1)配制碳酸钾、硫酸铵溶液.分别取碳酸钾和硫酸铵固体,加足量水搅拌. | 得到澄清溶液,温度无明显变化 | 得到澄清溶液,温度明显降低 | 都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量. |
| (2)猜想与假设. 碳酸钾、硫酸铵溶液的酸碱性都可能有种情况. 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液. | 变蓝 | 变红 | 说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 酸性. |
| (3)与盐酸反应. 分别取少量两种溶液于两只 试管中,加入稀盐酸. | 有气泡产生 | 无明显现象 | 碳酸钾能与酸反应. |
| (4)与氢氧化钠溶液反应. 分别取少量两种溶液于两只试管中,加入氢氧化钠溶液,微热. | 无明显现象 | 有气泡产生且有刺激性气味 | 硫酸铵能与碱反应.写出相关的化学方程式: (NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑ |
