题目内容
4.Fe2O3、CuO的混合粉末3.2g,高温下与足量H2充分反应后,得到固体的质量可能为( )| A. | 2.24g | B. | 2.56g | C. | 2.4g | D. | 4g |
分析 可以假设3.20g全部是氧化铁或氧化铜计算出铁元素或铜元素的质量,再进一步判断即可.
解答 解:3.20g氧化铁中铁元素的质量为:3.20g×$\frac{112}{160}$=2.24g,
3.20g氧化铜中铜元素的质量为:3.20g×$\frac{64}{80}$=2.56g,
由计算可知,高温下与足量H2充分反应后,得到固体的质量大于2.24g,小于2.56g,可能为2.40g.
故选:C.
点评 因为不知道氧化铁、氧化铜的质量分数,因此可以通过极值法计算出的结果进行判断,这是一种简洁的计算方法,要注意理解.

练习册系列答案
 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案
相关题目
12.下列不属于水的物理性质的是( )
| A. | 纯净的水是无色、无味的透明液体 | |
| B. | 水在4摄氏度时密度最大 | |
| C. | 在1000摄氏度以上,水蒸气可以分解 | |
| D. | 水是一种良好的溶剂,它能溶解多种物质 |
13.钠原子与钠离子相比,下列说法中正确的是( )
| A. | 核外电子数相同 | B. | 核内中子数不同 | C. | 电性相同 | D. | 属于同一种元素 |
14.如图所示图象能正确反映其对应关系的是( )
| A. |  向一定量pH=3的硫酸溶液中不断加水稀释 | |
| B. |  向一定量的饱和石灰水中不断加入生石灰 | |
| C. | 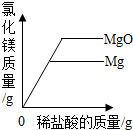 向盛有相同质量的镁和氧化镁的烧杯中分别加入相同溶质质量分数的稀盐酸至过量 | |
| D. |  将一定量的木炭放在盛有氧气的密闭容器中加热至燃烧 |